
下列说法正确的是
①煤经气化和液化两个化学变化过程,可变为清洁能源
②甲烷、乙烯和苯在工业上都可通过石油分馏得到
③食用白糖的主要成分是蔗糖
④用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
⑤乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
⑥纤维素、合成纤维、光导纤维都是有机高分子化合物
⑦制肥皂时,在皂化液里加入饱和食盐水,能够促进高级脂肪酸钠的析出
⑧苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理
⑨重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤
A.②④⑤⑦⑧ B.①③④⑦⑨
C.①⑤⑥⑧⑨ D.①②③⑤⑥
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:选择题
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )

A.该反应的化学方程式为3B+4C 6A+2D
6A+2D
B.反应进行到1s时,v(A)=v(C)
C.反应进行到6s时,B的平均反应速率为0.1 mol/(L•s)
D.反应进行到6s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关,下列说法正确的是( )
A.小苏打用于治疗胃溃疡病人的胃酸过多症
B.工厂常用的静电除尘方法与胶体性质无关
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
D.电解从海水中得到的氯化钠溶液可获得金属钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:选择题
分子式为C5H10O3的有机物与NaHCO3溶液反应时,生成C5H9O3Na;而与金属钠反应时生成C5H8O3Na2,则该有机物的同分异构体有( )种(不考虑立体异构)
A.10 B.11 C.12 D.13
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:选择题
高分子化合物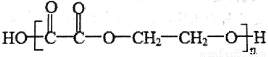 ,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
A.1-丁烯 B.乙炔 C.1, 3-丁二烯 D.乙烯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:填空题
已知有机化合物A、B、C、D、E存在下图所示转化关系,且C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的化合物。

请回答下列问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为_________________。
(2)B在一定条件下可以发生缩聚反应生成某高分子化合物,此高分子化合物的结构简式为_________________。
(3)C的核磁共振氢谱中有_________________个峰;D也可以由溴代烃F在NaOH溶液中加热来制取,写出此反应的化学方程式_________________。
(4)A的结构简式是_________________。
(5)B有多种同分异构体,请写出一种同时符合下列四个条件的结构简式:_________________。
a.能够发生水解 b.能发生银镜反应
c.能够与FeCl3溶液显紫色 d.苯环上的一氯代物只有一种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
某天然油脂10g,需2.52gKOH才能完全皂化,又知相同质量的该油脂催化加氢时消耗氢气0.15g,则1mol该油脂中含有碳碳双键( )
A.1.2mol B.3mol C.4mol D.5mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
下列关于有机化合物的认识不正确的是( )
A油脂在空气中完全燃烧转化为水和二氧化碳
B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异物体
C.在水溶液里,乙酸分子中的—CH3可以电离出H+
D.在浓硫酸存在下,苯与浓硝酸共热,生成硝基苯的反应属于取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分,其中的编号代表所对应的元素。请回答下列问题:

(1)⑧号元素的基态原子的价电子排布式是_________________,与其同周期,且基态原子的核外未成对电子数最多的元素是_______________(写出元素符号)。
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是_________________。
(3)①号与③号元素形成的含有18电子的分子为___________(写出名称),该分子中③元素的原子的杂化方式为______________。②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为______________(用对应的元素符号表示)。

(4)下表是某些短周期元素的电负性值:
元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
X值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.58 | 2.5 | 3.1 |
①通过分析电负性值变化规律,确定N最接近的电负性值范围:________<N<__________
②推测电负性值与原子半径关系是____________________;
③试判断:AlBr3中化学键类型是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com