
分析 (1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述;根据同一轨道的2两个电子自选方向相反判断;
(2)共价键为原子之间以共用电子对成键,碳的非金属性较弱,但半径较小,反应中难以失去或得到电子;
(3)CS2分子的结构式为S=C=S,含有δ键和π键;结合δ键和孤对电子数判断价层电子对数,以此判断杂化类型;
(4)熔点为253K,沸点为376K,具有分子晶体的性质;
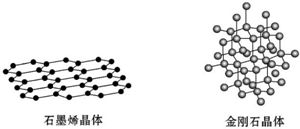
(5)石墨晶体中最小的环为六元环,每个碳原子连接3个C-C化学健,每个C-C化学健被2个碳原子共用.
解答 解:(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述,离核近的区域电子云密度较大,离核远的区域电子云密度较小,C原子核外电子排布为1s22s22p2,轨道式为如图所示: ,则在基态14C原子中,核外存在2对自旋相反的电子,
,则在基态14C原子中,核外存在2对自旋相反的电子,
故答案为:电子云;2;
(2)共价键为原子之间以共用电子对成键,碳原子核外有4个电子,且元素的非金属性较弱,但半径较小,反应中难以失去或得到电子,
故答案为:C原子最外层有4个电子,不易得失电子;
(3)CS2分子的结构式为S=C=S,含有δ键和π键,CS2分子中C原子形成2个δ键,孤对电子数为$\frac{4-2×2}{2}$=0,则为sp杂化,
故答案为:δ键和π键;sp;
(4)Fe(CO)5熔点为253K,沸点为376K,具有分子晶体的性质,则固体应为分子晶体,
故答案为:分子;
(5)石墨晶体中最小的环为六元环,每个碳原子连接3个C-C化学健,则每个C原子连接 3个六元环,每个六元环占有的C原子数为6×$\frac{1}{3}$=2,
故答案为:3;2.
点评 本题主要考查物质结构和性质,侧重考查学生空间想象能力、知识运用能力,涉及晶胞计算、原子结构等知识点,综合性较强,采用均摊法、价层电子对互斥理论等理论分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 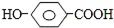 | B. | HO(CH2)2CHO | C. | HOOC-COOH | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该分子的摩尔质量约为40 | B. | 该分子由H2和O2构成 | ||
| C. | 1 mol该分子中含有22 mol中子 | D. | 1 mol该分子中含有20 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 装置 |  | 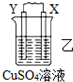 |  |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体发生 |
| A. | 装置甲中W作原电池负极 | |
| B. | 装置乙中Y电极上的反应式为Cu2++2e-=Cu | |
| C. | 装置丙中溶液的pH减小 | |
| D. | 四种金属的活动性强弱顺序为Z>W>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由非金属元素组成的化合物中一定不含离子键 | |
| B. | 离子化合物一定含有金属元素 | |
| C. | 分子中一定含有共价键 | |
| D. | 某种离子化合物可以同时含有离子键、极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性KMnO4溶液鉴别乙烯和乙炔 | |
| B. | 将铁屑、液溴、苯混合制溴苯 | |
| C. | 苯和溴苯采用分液的方法分离 | |
| D. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
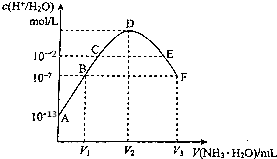
| A. | C点所示溶液中:pH=14-a | |
| B. | D点所示溶液中:c(H+)-c(OH-)=2c(NH3•H2O) | |
| C. | E点所示溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+) | |
| D. | F点所示溶液中:c(NH4+)=2c(SO42-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com