
���� ��1���÷�Ӧ�л�ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ����÷�Ӧ�з�Ӧ�����������붼�����壻
��2�����淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȡ��ٷֺ����Լ��ɴ������һϵ�����������䣻
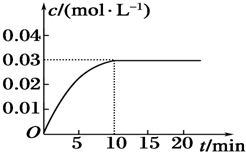
��3����һ���¶��£���ƽ�ⳣ��K=$\frac{1}{3}$�������ɵ�c��WI2��=xmol/L����μӷ�Ӧ��c��I2��=c��WI2��=xmol/L��ʣ���c��I2��=$\frac{1mol}{2L}$-xmol/L����ѧƽ�ⳣ��K=$\frac{x}{0.5-x}$=$\frac{1}{3}$��x=$\frac{1}{8}$����0-5min�ڵ�ƽ����Ӧ����v��WI2��=$\frac{��c}{��t}$��ƽ��ʱI2��g����ת����=$\frac{�μӷ�Ӧ��c��{I}_{2}��}{��ʼc��{I}_{2}��}��100%$��
��Ӧǰ���������ʵ������䣬����ⵥ�����ʵ���Ϊԭ����2����I2�����ʵ���Ũ��Ϊԭ����2����ƽ�ⳣ�����¶ȱ仯��Ũ������ﵽƽ���ʱ��̣����ﵽ��ƽ����ͬ��
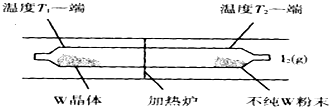
��4����ͼ��֪���ڸ��������µõ�����W���壬�������¶�ƽ�����淴Ӧ�����ƶ�����Ӧ��ϵ��I2��ѭ��ʹ�ã�
��� �⣺��1���÷�Ӧ�л�ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ����÷�Ӧ�з�Ӧ�����������붼�����壬���Ը÷�Ӧ��ѧƽ�ⳣ��K=$\frac{c��W{I}_{2}��}{c��{I}_{2}��}$��
�ʴ�Ϊ��$\frac{c��W{I}_{2}��}{c��{I}_{2}��}$��
��2��a��I2��g����WI2��g����Ũ�����ʱ�÷�Ӧ��һ���ﵽƽ��״̬���뷴Ӧ��ʼŨ�ȼ�ת�����йأ����Բ����ж�ƽ��״̬���ʴ���
b��W���������ٱ仯�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬������ȷ��
c����Ӧǰ�������ܶ����������ڻ��������ܶȱ��ֲ���ʱ�÷�Ӧ�ﵽƽ��״̬������ȷ��
d����Ӧǰ���������ʵ������䣬���������ڻ�������ѹǿʼ�ձ��ֲ��䣬���ܾݴ��ж�ƽ��״̬���ʴ���
��ѡbc��
��3����һ���¶��£���ƽ�ⳣ��K=$\frac{1}{3}$�������ɵ�c��WI2��=xmol/L����μӷ�Ӧ��c��I2��=c��WI2��=xmol/L��ʣ���c��I2��=$\frac{1mol}{2L}$-xmol/L����ѧƽ�ⳣ��K=$\frac{x}{0.5-x}$=$\frac{1}{3}$��x=$\frac{1}{8}$����0-5min�ڵ�ƽ����Ӧ����v��WI2��=$\frac{��c}{��t}$=$\frac{\frac{1}{8}mol/L}{5min}$=0.025 mol•L-1•min-1��ƽ��ʱI2��g����ת����=$\frac{�μӷ�Ӧ��c��{I}_{2}��}{��ʼc��{I}_{2}��}��100%$=$\frac{\frac{1}{8}mol}{0.5mol}��100%$=25%��
��Ӧǰ���������ʵ������䣬����ⵥ�����ʵ���Ϊԭ����2����I2�����ʵ���Ũ��Ϊԭ����2����ƽ�ⳣ�����¶ȱ仯��Ũ������ﵽƽ���ʱ��̣����ﵽ��ƽ����ͬ����ѡc��
�ʴ�Ϊ��0.025 mol•L-1•min-1��25%��c��
��4����ͼ��֪���ڸ��������µõ�����W���壬�������¶�ƽ�����淴Ӧ�����ƶ�������ӦΪ���ȷ�Ӧ������H��0��ͨ�������¶�T2�����ڷ�Ӧ������У�Ϊ���£��¶�T1�����ڷ�Ӧ������У�Ϊ���£�����T1��T2����Ӧ��ϵ��I2��ѭ��ʹ�ã�
�ʴ�Ϊ������I2��
���� ���⿼�黯ѧƽ����㡢��ѧƽ��״̬�жϡ���ѧƽ��Ӱ�����ص�֪ʶ�㣬���ؿ���ѧ����������������ע�⣺ֻ�з�Ӧǰ��ı��������������Ϊ��ѧƽ��״̬�ж����ݣ���Ӧǰ���������������Ϊ�ж����ݣ���Ŀ�ѶȲ���


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
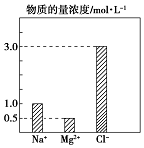 ij100mL��Һ�к��еIJ�������Ũ�ȴ�С��ͼ��ʾ������Һ���ܻ�����Fe3+��Ba2+��H+��SO42-��CO32-��Ϊ�˽�һ��ȷ�ϣ��Ը���Һ����ʵ���⣺
ij100mL��Һ�к��еIJ�������Ũ�ȴ�С��ͼ��ʾ������Һ���ܻ�����Fe3+��Ba2+��H+��SO42-��CO32-��Ϊ�˽�һ��ȷ�ϣ��Ը���Һ����ʵ���⣺| ʵ����������� | ʵ����� | �ж����� | |
| ����һ | ��ϸ�۲�����ͼ | �϶��� CO32- | �϶������ӵ�����̼������Ӻ�þ����֮��ᷴӦ |
| ����� | ����Һ����ɫ��������һ״̬ | �϶��� Fe3+ | �϶������ӵ����ɸ�����Ϊ��ɫ |
| ������ | ��������BaCl2��Һ������23.3g��ɫ�������ټ�ϡ���ᣬ��������ʧ | �϶���SO42-��H+���϶���Ba2+ | �϶���H+�����ɵ���غ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
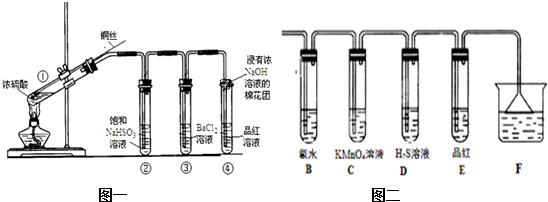
 ij����С����������װ�ã���Ũ�������Ҵ���Ӧ�Ŀ��ܲ������������̽����
ij����С����������װ�ã���Ũ�������Ҵ���Ӧ�Ŀ��ܲ������������̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
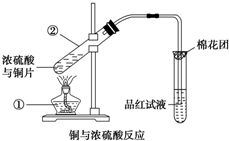 ��ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⣮
��ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | X | Y | 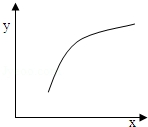 |
| A | �¶� | �����ڻ��������ܶ� | |
| B | A�����ʵ��� | B��ת���� | |
| C | ���������� | C��������� | |
| D | ����Ar�����ʵ��� | �淴Ӧ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʵ�鲻��Ҫָʾ�� | |
| B�� | ����Ͳ��ȡ������������ | |
| C�� | H2SO4��Ũ��Ϊ1.00 mol•L-1 | |
| D�� | �μӷ�Ӧ��H+��OH-�����ʵ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com