
在做化学实验时,我们经常遇到铁,请依据所学的知识回答下列问题:
(1)铁属于哪种类别的物质?
(2)在哪些实验中用到了铁?这些实验中铁发生了什么反应?试写出相关实验的化学方程式或结论。
(3)还有哪些物质可以代替铁完成这些实验?
(1)属于金属单质;(2)①在氧气或氯气中点燃:3Fe +2O2![]() Fe3O4,2Fe + 3Cl2
Fe3O4,2Fe + 3Cl2 ![]() 2FeCl3;②制取氢气:Fe +2HCl=FeCl2 + H2↑;③置换铜:Fe +CuSO4=FeSO4 + Cu;④在物理上测定导电性试验,铁是点的良导体等。(3)可以用锌、铝代替铁完成这些实验。
2FeCl3;②制取氢气:Fe +2HCl=FeCl2 + H2↑;③置换铜:Fe +CuSO4=FeSO4 + Cu;④在物理上测定导电性试验,铁是点的良导体等。(3)可以用锌、铝代替铁完成这些实验。
本题需要解决两个问题:一是铁有哪些性质,二是铁属于什么类别的物质。由于铁属于金属单质,则金属单质一般有4个通性,分别是:①与氧气反应生成金属氧化物,②与非氧气的非金属单质反应生成无氧酸盐,③与酸反应生成盐和氢气,④与盐溶液反应置换出较不活泼的金属单质。当然与之活泼性相近的金属锌、铝也具有此类的性质,故有时可用它们代替。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
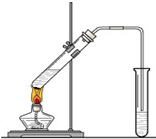 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 “酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.
“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯.| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
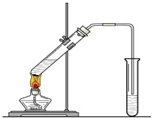 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
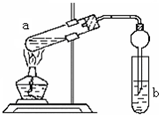 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com