

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2009?�Ͼ���ģ��ijͬѧ��Cu��HNO3�ķ�Ӧ��������̽������ش��й����⣮
��2009?�Ͼ���ģ��ijͬѧ��Cu��HNO3�ķ�Ӧ��������̽������ش��й����⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�갲��ʡ������ѧ��������Ծ������������ۺϻ�ѧ ���ͣ������
��11�֣�ij�о���ѧϰС��Ϊ̽��ͭ��п��Ũ����ķ�Ӧ�����ʵ��̽���������£�
ʵ����Ʒ����пƬ��ͭƬ��37%��Ũ���ᡢ����ˮ���Ȼ�����Һ��ϡ������Һ
ʵ���¼��
��Ӱ���ϣ�
|
|
| ���� | ��֤���� | Ԥ�������� |
| ��ΪͭƬ�п��ܺ���п������ | | |
| ���� | Ԥ����֤���� | �������������� |
| ��ɫ�������Ȼ���ͭ | | |
| | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡԥ�Ͼ�У�������Ĵ�������ѧ�Ծ� ���ͣ�ѡ����
ijͬѧ��������Ӧ��Ӧ�����ӷ���ʽ���������ۣ����к������� ( )
|
ѡ�� |
��ѧ��Ӧ |
���ӷ���ʽ |
���� |
|
A |
̼�����Ƶ�ˮ�� |
HCO3-+H2O |
��ȷ |
|
B |
��FeCl3��Һ�м���ͭ�� |
Cu + Fe3+ = Cu2++Fe2+ |
����ɲ��غ㡣 |
|
C |
��84����Һ������Ч�ɷ�ΪNaClO��Һ���͡�����顱 ���гɷ�ΪŨ���ᣩ��Ϸ� ������ |
ClO-+ Cl- + H+ = Cl2��+ OH- |
��ȷ |
|
D |
�����ʵ�����FeBr2��Cl2��Ӧ |
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
����Fe2+��Br- �����ʵ���֮���뻯ѧʽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���Ͼ���ģ ���ͣ������
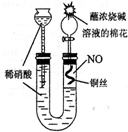
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com