
常温下,将a mol/L的NaOH溶液与0.1mol/L的稀硫酸按体积比19:11混合后溶液的pH=2。若将a mol/L的NaOH溶液逐滴加入到1L 0.1mol/L的磷酸溶液中,加入氢氧化钠溶液的体积与所得溶液pH的关系如下表:
| 加入NaOH溶液的体积 | pH | |
| ① | 0L | 2 |
| ② | 1L | 4 |
| ③ | 2L | 10 |
| ④ | 3L | 12 |
据此请回答:
(1)a = 。
(2) 溶液的pH由4升至10的过程中发生的主要反应的化学方程式为 ,pH=7时溶质成分的化学式为 。
(3)当溶液的pH=12时,加水稀释,溶液中c(Na+)/c(PO43-)的比值将 (填“增大”、“减小”、“不变”或“无法确定”)。
(4)将浓度均为0.1mol/L的Na2HPO4溶液和Na3PO4溶液混合后所得溶液中各离子浓度由大到小的顺序是 。
(5)在向磷酸溶液中滴加NaOH溶液的过程中,各离子浓度之间一定存在的等量关系式为
(加入的NaOH溶液的量大于零)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
可逆反应2NO2 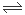 2NO + O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①混合物各物质的量的浓度相等 ②单位时间内生成n mol O2 的同时生成2n mol NO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的平均摩尔质量不再改变的状态
2NO + O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①混合物各物质的量的浓度相等 ②单位时间内生成n mol O2 的同时生成2n mol NO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的平均摩尔质量不再改变的状态
A.①④ B.①②③ C.②④⑥ D.①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
第三周期元素A、B、C,其原子序数依次增大,已知A的焰色为黄色,C的某种氧化物是形成酸雨的主要原因,且这三种元素的最高价氧化物的水化物有一种具有两性,且他们两两之间都能反应生成盐和水。
(1)填出元素符号A __________B __________C__________
(2) C 2- 离子结构示意图为
(3)A和C形成的化合物的电子式为 ,属于 化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
| 选项 | a中的物质 | b中的物质 | c中收集的气体 |
|
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,则下列说法正确的是( )
A.1mol FeCl3形成的 Fe(OH)3胶体中,胶体的颗粒为NA
B.标准状况下0.5mol NO和0.5mol O2组成的混合气体的体积约为22.4L
C.1molNa2O2与水反应时转移电子数约为NA
D.含1molHCl的浓盐酸与足量MnO2反应可制得0.25molCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程中,没有发生化学变化的是( )
A.干冰用于人工降雨
B.蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀
C.溶洞中钟乳石的形成
D.豆科作物的根瘤菌对空气中氮的固定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.H、D、T表示三种氢原子
B.原子最外层少于4个电子的元素均是金属元素
C.稀有气体元素最外层电子数均为8个
D.目前人们已发现了5000多种核素,说明发现了5000多种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式:
______________________________________________________________
(2)饱和碳酸钠溶液的主要作用是_____________________________________________。
(3)若要把制得的乙酸乙酯分离出来,应采用的实验操作是_____________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com