
已知氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物,且下列反应均可发生:(1)H2S+I2=2H++2I—+S¯ (2)H2SO3+2H2S=3S¯+3H2O (3)2I—+Br2=2Br—+I2
(4)H2SO3+I2+H2O=H2SO4+2HI 。则Br—、I—、H2S和H2SO3还原性由强到弱的顺序是( )
| A.H2S>H2SO3>I—>Br— | B.Br—>I—>H2SO3>H2S |
| C.H2SO3>H2S>Br—>I— | D.I—>Br—>H2S>H2SO3 |
科目:高中化学 来源: 题型:
126 53 |
127 53 |
128 53 |
131 53 |

- 3 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(分)物质A~E的转化关系如图所示:
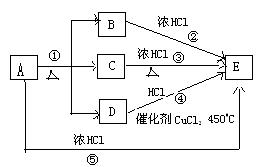
已知气体单质D能使带火星的木条复燃,反应①是实验室制单质D的常用方法之一,反应②是实验室制黄绿色气体E的重要反应,(部分生成物未列出)。
依据上述信息,回答下列问题:
(1)A的化学式
(2) 从氯元素化合价的变化看,以上写出反应②③④⑤四种方法的共同点是
(3)写出反应④的化学方程式
(4)利用反应③④⑤的变化,不写化学方程式比较A、C、D的氧化性由大到小的顺序
(5)写出反应②的离子方程式 ,氧化剂与还原剂的物质的量之比
查看答案和解析>>
科目:高中化学 来源: 题型:
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯(已知ClO2中
氯元素的化合价为+4价),其化学方程式为:
2KClO3+ 4HCl(浓) = 2KCl + 2ClO2↑ + Cl2↑ + 2H2O。
(1)浓盐酸在反应中表现出来的性质是 (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)该反应中:__________是氧化剂,__________是还原剂,__________元素被氧化,
__________元素被还原,__________是氧化产物,__________是还原产物,电子
转移总数为__________,当有1摩尔的氯气生成时,有__________摩尔的盐酸被
氧化,转移电子的物质的量为 mol。
(3)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1g质量的
物质得到的电子数)比Cl2 (填大、小或不变)。
查看答案和解析>>
科目:高中化学 来源:2010—2011学年广西北海市合浦县教研室高一上学期期末考试化学试卷 题型:填空题
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯(已知ClO2中 氯元素的化合价为+4价),其化学方程式为:
氯元素的化合价为+4价),其化学方程式为:
2KClO3 + 4HCl(浓) = 2KCl + 2ClO2↑ + Cl2↑ + 2H2O。
(1)浓盐酸在反应中表现出来的性质是 (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)该反应中:__________是氧化剂,__________是还原剂,__________元素被氧化,
__________元素被还原,__________是氧化产物,__________是还原产物,电子
转移总数为__________,当有1摩尔的氯气生成时,有__________摩尔的盐酸被
氧化,转移电子的物质的量为 mol。
(3)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1g质量的
物质 得到的电子数)比Cl2 (填大、小或不变)。
得到的电子数)比Cl2 (填大、小或不变)。
查看答案和解析>>
科目:高中化学 来源:2013届广西北海市合浦县教研室高一上学期期末考试化学试卷 题型:填空题
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯(已知ClO2中
氯元素的化合价为+4价),其化学方程式为:
2KClO3 + 4HCl(浓) = 2KCl + 2ClO2↑ + Cl2↑ + 2H2O。
(1)浓盐酸在反应中表现出来的性质是 (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)该反应中:__________是氧化剂,__________是还原剂,__________元素被氧化,
__________元素被还原,__________是氧化产物,__________是还原产物,电子
转移总数为__________,当有1摩尔的氯气生成时,有__________摩尔的盐酸被
氧化,转移电子的物质的量为 mol。
(3)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1g质量的
物质得到的电子数)比Cl2 (填大、小或不变)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com