
| A. | 标准状况下,22.4 L水中所含的分子数约为6.02×1023个 | |
| B. | 1 mol Cl2中含有的原子数为NA | |
| C. | 标准状况下,a L氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023个 | |
| D. | 常温常压下,11.2 L CO分子数是0.5NA |
分析 A.标准状况下,水的状态不是气体;
B.1mol氯气分子中含有2molCl;
C.氧气和氮气都是双原子分子,根据n=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$计算;
D.常温常压下,不是标况下,不能使用标况下的气体摩尔体积计算.
解答 解:A.标况下水不是气体,不能使用标况下的气体摩尔体积计算,故A错误;
B.1 mol Cl2中含有2mol氯原子,含有的原子数为2NA,故B错误;
C.标准状况下,a L氧气和氮气的混合物的物质的量为:$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,该混合气体中含有的分子数约为:$\frac{a}{22.4}$×6.02×1023个,故C正确;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算CO的物质的量,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与其它物理量之间的关系,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:实验题
(1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是 ,读数是_______℃;量筒应该是 ,读数为 mL;滴定管应该是 ,读数为 mL 。



(2)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是 。
①读取滴定管终点读数时,仰视刻度线。
②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失
③中和滴定时,锥形瓶内有少量蒸馏水。
④酸式滴定管用蒸馏水洗后,未用标准液洗。
⑤用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.68 g | B. | 6..68 g | ||
| C. | 2.34 g | D. | 由于m未知,无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
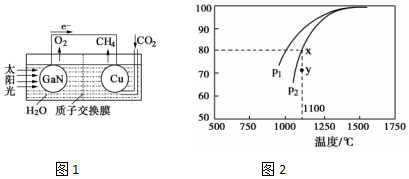 天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.
天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应大多数是放热反应,分解反应全都是吸热反应 | |
| B. | C(金刚石,s)+O2(g)=CO2(g)的反应热等于1molO2的键能与1molCO2中键能的差 | |
| C. | 热化学方程式中,反应条件可以不写,而且各物质前的化学计量数可以是分数 | |
| D. | 如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 饱和石灰水跟盐酸反应:H++OH-═H2O | |
| C. | 在硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 碳酸钙中加入盐酸:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用手接触药品 | |
| B. | 用一只酒精灯点燃另一只酒精灯 | |
| C. | 实验后,剩余的药品不能放回原瓶,也不能随便丢弃 | |
| D. | 将带有溶液的胶头滴管平放在实验台上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com