
| A. | 苯(苯酚):加NaOH溶液,充分振荡,分液,留下层液体 | |
| B. | 乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液即可 | |
| C. | 乙烷(乙烯):通过盛有足量酸性高锰酸钾溶液的洗气瓶洗气 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,留上层液体 |
分析 A.苯的密度比水小;
B.乙醛被氧化生成乙酸,乙醇、乙酸都溶于水;
C.乙烯被氧化生成二氧化碳气体;
D.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应.
解答 解:A.苯酚与氢氧化钠反应生成苯酚溶液,苯的密度比水小,在溶液的上层,应保留上层溶液,故A错误;
B.乙醛被氧化生成乙酸,乙醇、乙酸都溶于水,应用蒸馏的方法分离,故B错误;
C.乙烯被氧化生成二氧化碳气体,应用溴水除杂,故C错误;
D.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,可用分液的方法分离,故D正确.
故选D.
点评 本题考查混合物的分离,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同,为解答该题的关键,注意把握实验的可行性与合理性的评价,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
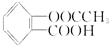 )与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
)与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )| A. | 1.5mol | B. | 2 mol | C. | 1 mol | D. | 0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
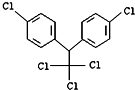
| A. | 它属于芳香烃 | B. | 1mol该物质能与6mol H2加成 | ||
| C. | 分子式为C14H8Cl5 | D. | 该有机易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0L1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 28g乙烯和丙烯的混合物含有的碳原子数为为2NA | |
| C. | 25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA | |
| D. | 1mol的羟基与1 mol的氢氧根离子所含电子数均为9NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,则其单体的结构简式为CH≡CH.
,则其单体的结构简式为CH≡CH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.02 mol•L-1•min-1 | |
| B. | 图Ⅱ所知反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 | |
| C. | 若在图Ⅰ所示的平衡状态下,再向体系中充入0.2molB和0.2molC,重新达到平衡前v(正)>v(逆) | |
| D. | 在200℃时,向容器中充入2mol A 和1mol B,达到平衡时,A 的体积分数大于0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com