
 碘在科研与生活中有重要应用.某兴趣小组用0.50mol•L-1KI、0.2%淀粉溶液、0.20mol•L-1K2S2O8、0.10mol•L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.已知:
碘在科研与生活中有重要应用.某兴趣小组用0.50mol•L-1KI、0.2%淀粉溶液、0.20mol•L-1K2S2O8、0.10mol•L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.已知:| 实验序号 | 体积/mL溶液 | ||||
| K2S2O8溶液 | H2O | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | V1 | V3 | 4.0 | 2.0 |
| ③ | 8.0 | V2 | V4 | V5 | 2.0 |
分析 (1)慢反应中有I2生成,使溶液变蓝色,而快反应中消耗I2,慢反应决定反应速率,慢反应中生成I2大于快反应中消耗的I2,可以观察到溶液变蓝色;
(2)实验目的是探究反应物浓度对化学反应速率的影响,由表中数据可知,KI溶液、Na2S2O3溶液用量相等,应是探究K2S2O8浓度对反应速率的影响,保持溶液总体积相等;
(3)保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短.
解答 解:(1)慢反应中有I2生成,使溶液变蓝色,而快反应中消耗I2,慢反应决定反应速率,当溶液中的 S2O32-或Na2S2O3耗尽后,碘才能与淀粉作用显示蓝色;
根据I2+2S2O32-═S4O62-+2I- (快)可知,1mol碘需2molS2O32-,根据方程式S2O82-+2I-═2SO42-+I2可知,生成1mol碘需为1molS2O82-,为确保能观察到蓝色,碘需有剩余,即n(S2O32-):n(S2O82-)<2:1,
故答案为:S2O32-或Na2S2O3;第一个;<2:1;
(2)实验目的是探究反应物浓度对化学反应速率的影响,由表中数据可知,KI溶液、Na2S2O3溶液用量相等,应是探究K2S2O8浓度对反应速率的影响,保持溶液总体积相等,即其他条件不变,只改变反应物K2S2O8浓度,从而才达到对照实验目的,故Vx=10.0mL-8.0mL=2.0mL,
故答案为:探究K2S2O8浓度对反应速率的影响,KI溶液、Na2S2O3溶液用量相等;2.0;保证溶液总体积不变,即其他条件不变,只改变反应物K2S2O8浓度,从而才达到对照实验目的;
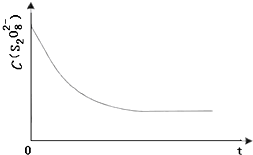
(3)保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短,降低反应温度和加入催化剂时c(S2O82-)~反应时间t的变化曲线示意图为: ,
,
故答案为: .
.
点评 本题考查反应速率影响因素的探究实验、化学计算等,(2)中注意利用控制变量法分析解答,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、HCO3-、NO3- | B. | Na+、SO42-、Cl-、S2- | ||
| C. | NH4+、Mg2+、SO42-、NO3- | D. | H+、K+、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能加快反应 | B. | 升高温度能增大反应的速率 | ||
| C. | 改变压强对反应速率没有影响 | D. | 降低温度能加快反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,46g有机物C2H6O中含有极性共价键的数目一定为7NA | |
| B. | 标准状况下,22.4L四氯化碳中所含有的共价键数目为4NA | |
| C. | 常温常压下,14g乙烯和丙烯的混合气体中含有的原子总数为3NA | |
| D. | 标准状况下,1mol苯分子中含有碳碳双键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子结构式:H-O-O-H | B. | 氚原子符号:${\;}_{1}^{2}$H | ||
| C. | Mg2+结构示意图: | D. | CO2的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
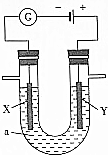 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
某无色溶液可能含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4- 中的几种。为确定其成分做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是
A.肯定有Al3+ 、Mg2+、NH4+、Cl- B.肯定有Al3+、Mg2+、HCO3-
C.肯定有K+、HCO3-、MnO4- D.肯定有Al3+、Mg2+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①③ | B. | 只有②③ | C. | 只有③④ | D. | 只有②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com