
| A. | 标准状况下,80gSO3的体积为22.4L | |
| B. | 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | |
| C. | 已知反应:2NH3+NO+NO2═2N2+3H2O,每生成28g N2转移的电子数目为3NA | |
| D. | 6.0gSiO2中含有0.1NA个 SiO2分子 |
分析 A、三氧化硫是固体,标准下气体摩尔体积不适用;
B.氯气与氢氧化钠溶液飞反应中,氯气既是氧化剂也是还原剂,属于歧化反应;
C、由反应2NH3+NO+NO2═2N2+3H2O可知生成2mol的氮气转移6mol的电子;
D、二氧化硅是原子晶体,构成微粒是原子.
解答 解:A、三氧化硫是固体,标准下气体摩尔体积不适用,故A错误;
B.标况下2.24L氯气的物质的量为0.1mol,氯气与氢氧化钠的反应是歧化反应,因此0.1mol氯气与氢氧化钠溶液反应转移了0.1mol电子,转移的电子总数为0.1NA,故B错误;
C、由反应2NH3+NO+NO2═2N2+3H2O可知生成2mol的氮气转移6mol的电子,所以每生成28g N2转移的电子数目为3NA,故C正确;
D、二氧化硅是原子晶体,构成微粒是原子,而不是分子.故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸可蚀刻玻璃说明氢氟酸具有强酸性 | |
| B. | 油脂的氢化说明油脂分子中含有不饱和键 | |
| C. | 维生素C常用作抗氧化剂说明它具有氧化性 | |
| D. | 汽车尾气中含有氮氧化物说明汽油中含有氮元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
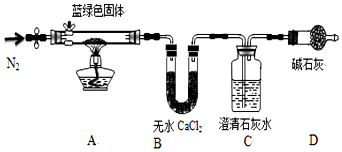
| 溶解度(s)/g | 溶度积(Ksp) | 摩尔质量(M)g/mol | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
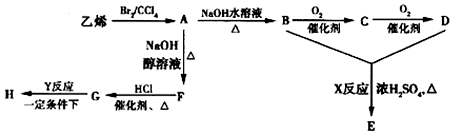
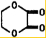 +2H2O;
+2H2O; +2NaOH$\stackrel{△}{→}$NaOOCCOONa+HOCH2CH2OH.
+2NaOH$\stackrel{△}{→}$NaOOCCOONa+HOCH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷与氯气光照反应可以制得较纯净的1,2-二氯乙烷 | |
| B. | 苯中的化学键都是非极性键 | |
| C. | 煤的干馏属于物理变化 | |
| D. | 涤纶、酚醛树脂和蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
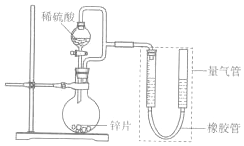 某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:
某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究:| 序号 | V(H2SO4)/mL | C(H2SO4)/mol•L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂 | |
| B. | 为了防止蛋白质盐析,疫苗等生物制剂应冷冻保藏 | |
| C. | 溴化银见光易分解,可用作胶片感光剂 | |
| D. | 硅胶多孔,常用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | R的核电荷数是43 | |
| B. | R的最高正化合价为+3价 | |
| C. | R的最高价氧化物对应水化物的酸性比硝酸弱 | |
| D. | 气态氢化物的稳定性:NH3<RH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com