
 ¢Åø÷Č”ŹŹĮæ¹ĢĢåŹŌ¼Į·Ö±š¼ÓČė5Ö§ŹŌ¹ÜÖŠ£¬
¢Åø÷Č”ŹŹĮæ¹ĢĢåŹŌ¼Į·Ö±š¼ÓČė5Ö§ŹŌ¹ÜÖŠ£¬ ¼ÓČėŹŹĮæÕōĮóĖ®£¬Õńµ“ŹŌ¹Ü£¬¹Ū²ģŌņ ±»¼ģ³öµÄĪļÖŹµÄ»ÆѧŹ½ŹĒ
¼ÓČėŹŹĮæÕōĮóĖ®£¬Õńµ“ŹŌ¹Ü£¬¹Ū²ģŌņ ±»¼ģ³öµÄĪļÖŹµÄ»ÆѧŹ½ŹĒ  ¢Ę·Ö±šČ”Ī“¼ģ³öŅŗ£¬ĶłĘäÖŠ¼ÓČėÉĻŹöŅŃ¼ģ³öµÄČÜŅŗ£¬¹Ū²ģµ½µÄĻÖĻóŗĶĻąÓ¦µÄĄė×Ó·½³ĢŹ½£ŗ
¢Ę·Ö±šČ”Ī“¼ģ³öŅŗ£¬ĶłĘäÖŠ¼ÓČėÉĻŹöŅŃ¼ģ³öµÄČÜŅŗ£¬¹Ū²ģµ½µÄĻÖĻóŗĶĻąÓ¦µÄĄė×Ó·½³ĢŹ½£ŗ ¢ŁĻÖĻó£ŗŹŌ¹ÜÖŠÓŠ°×É«³ĮµķÉś³É£¬Ąė×Ó·½³ĢŹ½£ŗ £»
¢ŁĻÖĻó£ŗŹŌ¹ÜÖŠÓŠ°×É«³ĮµķÉś³É£¬Ąė×Ó·½³ĢŹ½£ŗ £» ¢ŚĻÖĻó£ŗŹŌ¹ÜÖŠÓŠĄ¶É«³ĮµķÉś³É£¬Ąė×Ó·½³ĢŹ½£ŗ £»
¢ŚĻÖĻó£ŗŹŌ¹ÜÖŠÓŠĄ¶É«³ĮµķÉś³É£¬Ąė×Ó·½³ĢŹ½£ŗ £»
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ü | B£®¢Ł¢Ū | C£®¢Ł¢Ū¢Ü | D£®¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 Ļ”ĮņĖįÖŠ£¬ČÜŅŗĄļ Ąė×ÓµÄĮæ¼õÉŁ£¬ Ąė×ÓµÄĮæŌö¼Ó£¬ Ąė×ÓµÄĮæƻӊ±ä»Æ.
Ļ”ĮņĖįÖŠ£¬ČÜŅŗĄļ Ąė×ÓµÄĮæ¼õÉŁ£¬ Ąė×ÓµÄĮæŌö¼Ó£¬ Ąė×ÓµÄĮæƻӊ±ä»Æ. ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ļņ0.1mol”¤L£1 Na2CO3ČÜŅŗÖŠµĪ¼Ó·ÓĢŖ£¬ČÜŅŗ±äŗģÉ« |
| B£®³£ĪĀĻĀÓÉĖ®µēĄė³öĄ“µÄc(H+) =10-13mol/LµÄČÜŅŗ£ŗ K+”¢HS-”¢Br-”¢Ba2+ |
| C£®½«1mol FeCl3Č«²æ×Ŗ»Æ³É½ŗĢå,ĘäÖŠĒāŃõ»ÆĢś½ŗĮ£ŹżĪŖNA |
| D£®0.lmol/L Fe2(SO4)3ČÜŅŗÖŠŅõĄė×ÓŗĶŃōĄė×Ó×ÜŹżµČÓŚ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 ×ÓµÄÅضČČēĻĀ±ķ£¬ŌņMĄė×ÓæÉÄÜĪŖ:
×ÓµÄÅضČČēĻĀ±ķ£¬ŌņMĄė×ÓæÉÄÜĪŖ:| Ėłŗ¬Ąė×Ó | NO3£ | SO42£ | H+ | M |
| ÅØ¶Č /£Ømol”¤L£1£© | 2 | 1 | 2 | 1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| æÉÄÜ“óĮæŗ¬ÓŠµÄŃōĄė×Ó | H+ NH4+ Al3+ K+ |
| æÉÄÜ“óĮæŗ¬ÓŠµÄŅõĄė×Ó | Cl- Br- I? ClO? AlO2- |
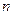 £©Óė¼ÓČėNaOHČÜŅŗµÄĢå»ż£Ø
£©Óė¼ÓČėNaOHČÜŅŗµÄĢå»ż£Ø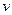 £©µÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£
£©µÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£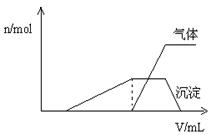
 __ ___ __£»
__ ___ __£» Cl£ ”¢Br£”¢I££¬ČōĻņ1 LøĆ»ģŗĻČÜŅŗÖŠĶØČėŅ»¶ØĮæµÄCl2£¬ČÜŅŗÖŠCl£”¢Br£”¢I£µÄĪļÖŹµÄĮæÓėĶØČėCl2µÄĢå»ż±ź×¼×“æö£©µÄ¹ŲĻµČēĻĀ±ķĖłŹ¾£¬·ÖĪöŗó»Ų“šĻĀĮŠĪŹĢā£ŗ
Cl£ ”¢Br£”¢I££¬ČōĻņ1 LøĆ»ģŗĻČÜŅŗÖŠĶØČėŅ»¶ØĮæµÄCl2£¬ČÜŅŗÖŠCl£”¢Br£”¢I£µÄĪļÖŹµÄĮæÓėĶØČėCl2µÄĢå»ż±ź×¼×“æö£©µÄ¹ŲĻµČēĻĀ±ķĖłŹ¾£¬·ÖĪöŗó»Ų“šĻĀĮŠĪŹĢā£ŗ| Cl2µÄĢå»ż£Ø±ź×¼×“æö£© | 2£®8L | 5£®6 L | 11£®2 L |
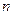 £ØCl££© £ØCl££© | 1£®25mol | 1£®5 mol | 2 mol |
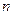 £ØBr££© £ØBr££© | 1£®5 mol | 1£®4 mol | 0£®9 mol |
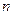 £ØI££© £ØI££© | 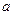 mol mol |  0 0 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®KCl£¬NaHSO4 | B£®KCl£¬Na2SO4£¬NaCl |
| C£®NaCl£¬KCl£¬K2SO4 | D£®KCl£¬K2SO4£¬Na2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
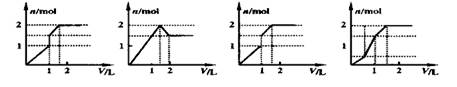
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com