有机物A(含C、H、O三种元素)与CH3COOH无论以何种比例混合,只要混合物总质量不变,完全燃烧后产生的水的质量也不变.试回答下列问题:
(1)符合条件的A的必要条件是:______.
(2)符合条件的相对分子量最小的有机物A是______(写结构简式)
(3)若A中C、H元素质量分数之和为86.67%,其余为O,A的相对分子量小于200,则A的分子式为______.如果A中含苯环结构且能发生银镜反应,符合条件的A的同分异构体有(写出一个即可):______.含1.8gA的溶液与足量银氨溶液发生银镜反应生成银的质量为______g.
【答案】
分析:(1)有机物A(含C、H、O三种元素)与CH
3COOH无论以何种比例混合,只要混合物总质量不变,完全燃烧后产生的水的质量也不变,说明H元素质量分数为定值,则有机物A中氢元素质量分数为
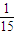
;
(2)CH
3COOH的最简式为CH
2O,与甲醛的分子式相同;
(3)计算氧元素的质量分数,进而计算氧原子最大数目,确定含有O原子数目,再计算有机物的相对分子质量,进而计算分子中H、C原子数数目,确定分子式;
如果A中含苯环结构且能发生银镜反应,则含有醛基或为甲酸形成的酯,结合有机物的分子式确定其结构,进而根据醛基与Ag按物质的量之比为1:2的关系计算生成Ag的质量.
解答:解:(1)有机物A(含C、H、O三种元素)与CH
3COOH无论以何种比例混合,只要混合物总质量不变,完全燃烧后产生的水的质量也不变,则有机物A中氢元素质量分数为
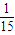
,
故答案为:有机物A中氢元素质量分数为
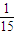
;
(2)CH
3COOH的最简式为CH
2O,与甲醛的分子式相同,故符合条件的相对分子量最小的有机物A是HCHO,
故答案为:HCHO;
(3)氧元素的质量分数=1-86.67%=13.33%,A的相对分子量小于200,A分子中最大氧原子数目=
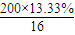
=1.7,故A含有1个氧原子,则A的相对分子质量=
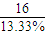
=120,则A分子中N(H)=
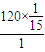
=8,N(C)=
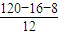
=8,故A的分子式为C
8H
8O;
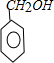
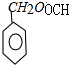
如果A中含苯环结构且能发生银镜反应,则含有醛基,故符合条件的A的结构为:
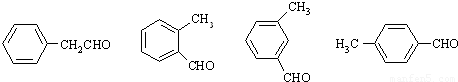
;
由于醛基与Ag按物质的量之比为1:2的关系进行,则:
C
8H
8O~2Ag
120 216
1.8g m
故m=
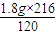
=3.24g
故答案为:C
8H
8O;
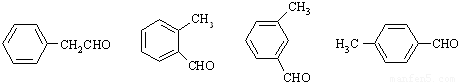
任意一个;3.24.
点评:考查有机物结构式的确定与性质,难度中等,注意判断有机物A中氢元素的质量分数与乙酸中氢元素的质量分数相等,确定A分子中氧原子数目是关键.

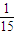 ;
;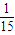 ,
,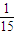 ;
;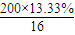 =1.7,故A含有1个氧原子,则A的相对分子质量=
=1.7,故A含有1个氧原子,则A的相对分子质量=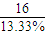 =120,则A分子中N(H)=
=120,则A分子中N(H)=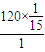 =8,N(C)=
=8,N(C)=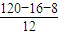 =8,故A的分子式为C8H8O;
=8,故A的分子式为C8H8O; ;
;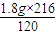 =3.24g
=3.24g 任意一个;3.24.
任意一个;3.24.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案










 +H2O
+H2O
 +H2O
+H2O



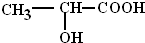 俗称乳酸,乳酸经过聚合制得的聚乳酸树脂,可以广泛用于医疗、包装、纺织等行业. 若用丙烯(其他无机试剂任选)为原料合成乳酸,合成过程中涉及到的反应类型依次是
俗称乳酸,乳酸经过聚合制得的聚乳酸树脂,可以广泛用于医疗、包装、纺织等行业. 若用丙烯(其他无机试剂任选)为原料合成乳酸,合成过程中涉及到的反应类型依次是

