
分(I)A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素.F与G位置相邻.G是同周期元素中原子半径最小的元素。
请用化学用语回答:
(1)A与D形成的18电子的化合物与FD2化合生成一种强酸,写出该强酸酸式钠盐水溶液的电离方程式为:________________。
(2)用电子式表示化合物E2D的形成过程:________________。
(3)在l0lkPa、25℃下,14g气态B2A4在D2中完全燃烧,放出QkJ热量,则B2A4的燃烧热的热化学方程式为:________________。
(Ⅱ)A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去)
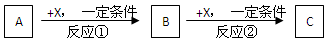
试同答:
(4)若X是强氧化性单质,则A不可能是___________。
a.H,S b. NH3c.Na d.Zn e.CH3CH2OH
(5)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则C的化学式为________________。
(6)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为______________。
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
已知 25 ℃时部分弱电解质的电离平衡常数数据如下表:

回答下列问题:
(1)写出碳酸的主要的电离方程式 。若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+) 原来的十分之一(填“大于”、“小于”或“等于”).
(2))物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为 (用编号填写)。
a.CH3COONa b. Na2CO3 c. NaClO d.NaHCO3 e.NaSCN
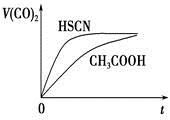
(3)25℃时,将 20mL0.1mol·L-1CH COOH 溶液和 20mL0.1mol·L-1HSCN 溶液分别与 20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图。反应初始阶段两种溶液产生 CO2 气体的速率存在明显差异的原因是 反应结束后,假设 NaHCO3 完全反应且气体全部逸出,则所得两溶液中,c(CH3COO-) _c(SCN-)(填“>”、“<”或“=”;)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)―c(CH3COO-)=_ mol/L(填代入数据后的计算式,不必算出具体数值)。
(5)向 NaClO 溶液中通入少量的 CO2,发生反应的离子方程式为 __________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上期中化学试卷(解析版) 题型:选择题
化学家借助太阳能产生的电能和热能,用空气和水作原料成功地合成了氨气。下列有关说法正确的是( )
A.该合成中所有的电能和热能全部转化为化学能
B.该合成氨过程不属于氮的固定
C.空气、水、太阳能均为可再生资源
D.断裂N2中的N≡N键会释放出能量
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三上学期一检化学试卷(解析版) 题型:简答题
工业上用硫铁矿石(主要成分FeS2)在沸腾炉中焙烧,经过一系列反应,得到硫酸,焙烧后的矿渣用于炼铁。其转化过程如下图所示(部分条件、反应物和产物已略去):
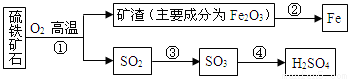
请回答下列问题:
(1)在上面转化过程中,硫元素被氧化的反应是________(填反应编号)。
(2)写出反应②中炼铁的化学方程式_____________。若用1000t含杂质28%的矿渣炼铁,理论上可得到含铁96%的生铁质量为_____________ t.
(3)写出反应①的化学方程式 ,若有12.0g FeS2参加反应,则发生转移的电子数为 。
(4)烟气中SO2的排放会造成酸雨,工业上常用Na2SO3溶液来吸收SO2以减少对环境的危害。
①常温下,将SO2通入一定体积的1.0mol·L-1Na2SO3溶液中,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,此时溶液中c(SO32-)的浓度是0.2mol·L-1,则溶液中c(HSO3-)是 mol·L-1。用化学平衡原理解释此时溶液显酸性的原因 。
②向①中pH约为6时的吸收液中通入足量O2充分反应。取反应后溶液10mL与10mLBaCl2溶液混合,欲使混合时能生成沉淀,所用BaCl2溶液的浓度不得低于 mol·L-1。[已知25℃时,Ksp(BaSO3)=5.48×10-7 , Ksp(BaSO4)= 1.08×10-10]
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市高三上学期一检化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关,下列说法正确的是
A. 煤的干馏可得到煤油、石蜡和沥青
B. 自来水厂可用明矾对水进行消毒杀菌
C. 氧化铝可用来制造耐高温的容器
D. 装有硅胶的透气袋可防止富含油脂的月饼被氧化
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:选择题
某固体混合物可能由Al2(NH4)2SO4、MgCl2、FeCl2、AlC13中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是

A.一定含有Al,其质量为4.5g
B.一定不含FeCl2,可能含有MgCl2和AIC13
C.一定含有MgCl2和FeCl2
D.一定含有(NH4)2SO4和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源:2017届湖南省郴州市高三上第二次教学质量监测化学卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.NaAl(SO4)2溶液中滴加Ba(OH)2直至SO42-沉淀完全:
2Al3++ 6OH-+ 3SO42-+ 3Ba2+= 2Al(OH)3↓+3BaSO4↓
B.NH4HS溶液与少量的NaOH溶液反应:NH4++ OH-= NH3·H2O
C.稀H2SO4和Na2S2O3溶液共热:S2O32-+2H+=SO2↑+S↓+H2O
D.过量Cl2通入FeI2溶液中:3C12+2I-+ 4Fe2+= 4C1-+I2+4Fe3+
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省铁岭市协作体高三上联考四化学试卷(解析版) 题型:选择题
被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A. 原子半径:Y>Z>R>T
B. 气态氢化物的稳定性:W<R<T
C. 最高价氧化物对应的水化物的碱性:X>Z
D. XR2、WR2两种化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一12月月考化学试卷(解析版) 题型:选择题
将0.01 molNaOH和0.01 molNa2CO3混合并配成溶液,向溶液中滴加0.1mol/L稀盐酸。下列图象能正确表示加人盐酸的体积和生成CO2的物质的量的关系的是( )
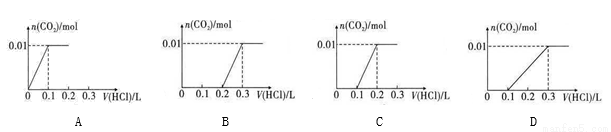
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com