
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 反应至6min时,c(H2O2)=0.20mol/L | |
| B. | 反应至6min时,H2O2分解了40% | |
| C. | 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| D. | 6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min) |
分析 A.由A计算可知6min内过氧化氢浓度变化量,6min时的浓度=起始浓度-浓度变化量;
B.H2O2分解率=(H2O2浓度变化量÷H2O2起始浓度)×100%.C.0~6min时间内,生成氧气为 $\frac{0.0224L}{22.4L/mol}$=0.001mol,则△c(H2O2)=0.002mol÷0.01L=0.2mol/L,根据v=$\frac{△c}{△t}$计算v(H2O2);
D.随着反应的进行,H2O2的浓度逐渐减小,反应速率减慢,6~10min的平均反应速率小于0~6min时间内反应速率.
解答 解:A.由A计算可知,反应至6 min时c(H2O2)=0.4mol/L-0.2mol/L=0.2mol/L,故A正确;
B.6min内△c(H2O2)=0.2mol/L,则H2O2分解率为:$\frac{0.2mol/L}{0.4mol/L}$×100%=50%,故B错误;
C.0~6min时间内,生成氧气为 $\frac{0.0224L}{22.4L/mol}$=0.001mol,由2H2O2 $\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,可知△c(H2O2)=0.001mol×2÷0.01L=0.2mol/L,所以v(H2O2)=0.2mol/L÷6min≈0.033mol/(L•min),故C正确;
D.随着反应的进行,H2O2的浓度逐渐减小,反应速率减慢,6~10min的平均反应速率小于0~6min时间内反应速率,故D正确;
故选B.
点评 本题考查化学平衡有关计算、化学反应速率计算、化学反应速率影响因素等,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| 实验编号 | C(HA)mol•L-1 | c(MOH)/mol•L-1 | 混合溶液的pH |
| 甲 | pH=2 | pH=12 | pH<7 |
| 乙 | 0.1 | 0.1 | pH=a |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
| A. | a>7 | |
| B. | 在乙组混合液中c(OH-)-c(HA)=10-amol/L | |
| C. | c1<0.2 | |
| D. | 在丁组混合液中c(M+)>c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
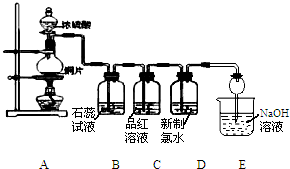 某化学兴趣小组为探究SO2的化学性质,设计了如图所示的装置进行实验.回答下列问题:
某化学兴趣小组为探究SO2的化学性质,设计了如图所示的装置进行实验.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电离方程式可写作H2O2?H++HO2-,HO2-?H++O22- | |
| B. | 加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大 | |
| C. | 加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动 | |
| D. | 加入少量氯化铁溶液,溶液中产生大量气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液 | B. | 胶体 | C. | 悬浊液 | D. | 乳浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子质量 | B. | 质量 | C. | 密度 | D. | 原子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com