
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.新制氯水与碳酸氢钠不反应 |
| B.25℃时,0.1mol/L的醋酸溶液与0.01mol/L的醋酸溶液中,Ka前者小于后者 |
| C.NaClO溶液中通入少量二氧化碳的反应为:2NaClO+CO2+ H2O = Na2CO3 +2HClO |
| D.等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)=c(CHCOO-)+c(OH-) |
| B.加入少量CH3COONa固体后,加入,c(CH3COO-)降低 |
| C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/L |
| D.与等体积pH =11的NaOH溶液混合后所得溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+) | B.Ka(HF) |
| C.c(F-)/c(H+) | D.c(H+)/c(HF) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.弱碱的浓度大于强酸的浓度 |
| B.反应完全后的溶液呈碱性 |
| C.原氨水中有1%的含氮微粒为NH4+ |
| D.反应后的溶液中NH4+、NH3·H2O与NH3三种微粒的平衡浓度之和为0.05 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+) | B.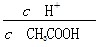 |
| C.c(H+)·c(OH-) | D.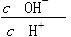 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质在水溶液中完全电离成阴、阳离子 |
| B.在溶液中,导电能力强的电解质是强电解质 |
| C.对同一弱电解质来说,当溶液的温度和浓度不同时,其导电能力也不相同 |
| D.纯净的强电解质在液态时,有的导电,有的不导电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com