
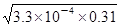 =1×10-2mol/L,pH=1,故A正确;B、电离常数只受温度的影响,不随浓度的变化而变化,故B错误;C、0.31 mol/L的HF溶液中c(H+)=c(F-)=1×10-2mol/L。故C错误;在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合后c(F-)=0.5×10-2mol/L,c(Ca2+)=0.001mol/L,则c2(F-)×c(Ca2+)=(0.5×10-2)2×0.001=2.5×10-8>1.46×10-10,因此该体系中有CaF2沉淀产生,故C不正确。D、向饱和的CaF2溶液中加水后,溶液还可能是饱和的,所以c(Ca2+)不一定比加水前减小,D不正确,答案选A。
=1×10-2mol/L,pH=1,故A正确;B、电离常数只受温度的影响,不随浓度的变化而变化,故B错误;C、0.31 mol/L的HF溶液中c(H+)=c(F-)=1×10-2mol/L。故C错误;在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合后c(F-)=0.5×10-2mol/L,c(Ca2+)=0.001mol/L,则c2(F-)×c(Ca2+)=(0.5×10-2)2×0.001=2.5×10-8>1.46×10-10,因此该体系中有CaF2沉淀产生,故C不正确。D、向饱和的CaF2溶液中加水后,溶液还可能是饱和的,所以c(Ca2+)不一定比加水前减小,D不正确,答案选A。

科目:高中化学 来源: 题型:
 (2011?深圳一模)氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.
(2011?深圳一模)氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.查看答案和解析>>
科目:高中化学 来源:四川省攀枝花市2012-2013学年高一下学期期末调研监测化学试题 题型:013
|
已知某温度下,几种酸的电离常数如下:K(HCN)=6.2×10-10、K(HF)=6.8×10-4、K(CH3COOH)=1.8×10-5、K(HNO2)=6.4×10-6.则物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是 | |
| [ ] | |
A. |
NaCN |
B. |
NaF |
C. |
CH3COONa |
D. |
NaNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
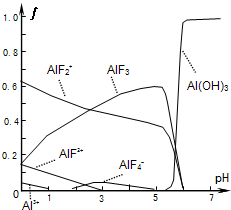 氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.
氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.查看答案和解析>>
科目:高中化学 来源:2011年广东省深圳市高考化学一模试卷(解析版) 题型:填空题
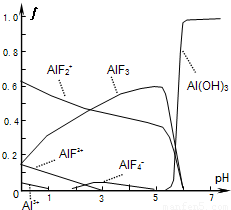
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com