
| A. | 分子中含有两个氢原子的酸一定是二元酸 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | Na2O、Na2O2组成元素相同,与CO2反应产物相同 | |
| D. | 钢铁发生电化学腐蚀时,负极的电极反应式为Fe-3e-═Fe3+ |
分析 A.能电离出的氢离子显酸性,分子中含有两个氢原子的酸不一定是二元酸;
B.胶体不能透过半透膜;
C.Na2O与CO2发生化合反应、Na2O2与CO2发生氧化还原反应;
D.铁在负极失电子生成亚铁离子.
解答 解:A.能电离出的氢离子显酸性,分子中含有两个氢原子的酸不一定是二元酸,如HCOOH属于一元酸,故A错误;
B.血液是胶体,胶体不能透过半透膜,所以“血液透析”利用了胶体的性质,故B正确;
C.Na2O与CO2发生化合反应生成碳酸钠,Na2O2与CO2发生氧化还原反应生成碳酸钠和氧气,反应产物不同,故C错误;
D.铁在负极失电子生成亚铁离子,则钢铁发生电化学腐蚀时,负极的电极反应式为Fe-2e-═Fe2+,故D错误.
故选B.
点评 本题考查了物质的分类、氧化还原反应、钠元素的化合物的性质、电极方程式的书写,题目涉及的知识点较多,侧重于基础知识的综合应用的考查,题目难度中等.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 2F2+2H2O═4HF+O2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
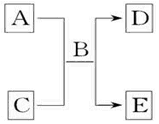 A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:
A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
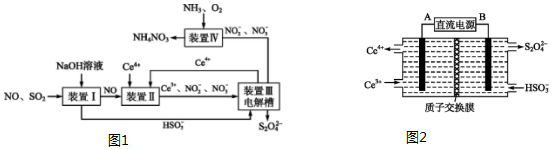
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与盐酸反应,铁合金不与盐酸反应 | |
| B. | 一定条件下,铁粉可与水蒸气反应生成四氧化三铁和氢气 | |
| C. | 不锈钢是铁合金,只含金属元素 | |
| D. | 纯铁的硬度和熔点均低于铁合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O所含的水分子数为NA | |
| B. | 常温常压下,16 g氧气所占的体积为11.2 L | |
| C. | 同温同压下,1 mol任何物质所占的体积相等 | |
| D. | 标准状况下,2NA个二氧化碳分子所占的体积为44.8 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com