
【题目】镁铝合金因坚硬、轻巧、美观、易于加工而成为被广泛应用的新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是
A. 不易生锈 B. 导电性好
C. 密度较小 D. 强度较高
科目:高中化学 来源: 题型:
【题目】M元素的一个原子失去两个电子转移到R元素的两个原子中去,形成离子化合物。下列四种化合物都符合条件,但从结构上看,有一种物质与其它三种明显不同,该物质是( )
A. FeS2 B. CaC2 C. BaO2 D. MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进入20世纪以后,化学科学经历了迅速发展的“创新百年”。下列各项中,不属于这个时期的化学重大成就的是
A. 制陶技术的成熟应用 B. 现代量子化学理论的建立
C. 化学工业的迅速发展 D. 放射性元素的发现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是含氮量最高的氮肥。
(1) 已知工业上合成尿素的反应分为如下两步:
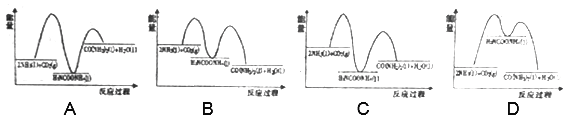
第1步:2NH3(I)+CO2(g) ![]() H2NCOONH4(I) H1=-330.0kJ·mol-1
H2NCOONH4(I) H1=-330.0kJ·mol-1
第2步:H2NCOONH4(I) ![]() H2O(I)+CO(NH2)2(I) H2=+226.3 kJ·mol-1
H2O(I)+CO(NH2)2(I) H2=+226.3 kJ·mol-1
则下列各图能正确表示尿素合成过程中能量变化曲线的是___________(填字母编号)。
(2)一定条件下工业合成尿素的总反应:CO2(g)+2HH3(g) ![]() CO(NH2)2(g)+H2O(g),t℃时,向容积恒定为2L的密闭容器中加入0.20molCO2和0.80molNH3,反应中CO2的物质的量随时间变化如下表所示:
CO(NH2)2(g)+H2O(g),t℃时,向容积恒定为2L的密闭容器中加入0.20molCO2和0.80molNH3,反应中CO2的物质的量随时间变化如下表所示:
时间/min | 0 | 40 | 70 | 80 | 100 |
n(CO2)/mol | 0.20 | 0.12 | 0.10 | 0.10 | 0.10 |
①前40min内v(NH3)=_________,此温度下该反应的平衡常数为___________。
②30min时v正(CO2)________80min时v逆(H2O)(选填“>”、“=”、“<”)。
③在100min时,保持其它条件不变,再向容器中充入0.10molCO2和0.4molNH3,重新建立平衡后CO2的转化率与原平衡相比将________(填“增大”、“不变”、“减小”)
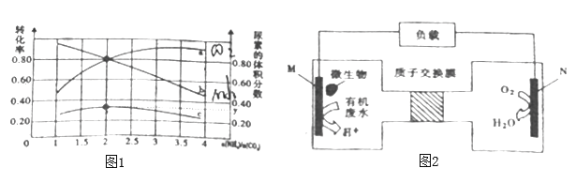
④氨碳比[n(NH3)/n(CO2)]对合成尿素有影响,恒温恒容条件下将总物质的量为3mol的NH3和CO2的混合气体按不同氨碳比进行反应,结果如图1所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平和体系中尿素的体积分数变化。[n(NH3)/n(CO2)]=______时,尿素产量最大,经计算图中y=_______(精确到0.01)。
(3)工业生成中为提高尿素的产率可采取的措施有___________________。
(4)近期科学家发现微生物可将生产废水中的尿素直接转化为对环境友好的两种物质,其工作原理如图2所示。回答下列问题:
①N极为_________极(填“正”、“负”),M电极反应式________________。
②N极消耗标准状况下33.6L气体时,M极理论上处理的尿素的质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠呦呦因发现青蒿素治疗疟疾新方法而获得2015年诺贝尔生理学奖。这是中国本土培养的科学家首次获得诺贝尔奖。请回答下列有关问题:
(1)青蒿素的分子式为C15H22O5,其组成中的三种元素的电负性有大大小排序是_______,其中第一电离能最大元素基态原子的核外电子排布式为______________。
(2)在确定青蒿素结构的过程中,可采用KBH4作为还原剂,其制备流程如下:

①已知金属晶体Na的配位数为8,则其晶胞结构图符合图1的_____________(选填字母编号),其堆积方式为_______(填名称)

②图2是NaH的晶胞结构,则NaH晶胞中Na+的数目为_________,若该晶体密度为ρg·cm-3,则晶胞中相距最近的两个Na+间的距离为________cm(用含ρ、NA的代数式表示)。
③化合物B(OCH3)3中C的杂化轨道类型为________,B(OCH3)3的空间构型为________,与其具有相同空间构型的分子和离子有________、_________(分子或离职各写一种)。
④KBH4的电子式__________,晶体结构中存在的作用力有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 纳米材料是指一种称为“纳米”的新物质制成的材料
B. 绿色食品是指不含任何化学物质的食品
C. 生物固氮是指植物通过叶面直接吸收空气中的氮气
D. 光导纤维是以二氧化硅为主要原料制成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 氯苯在NaOH的醇溶液中加热能发生消去反应
B. 通过核磁共振氢谱可以区分乙醇和乙酸乙酯
C. 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有5种
D. 苯酚与苯甲醇( )分子组成相差一个CH2原子团,因而它们互为同系物
)分子组成相差一个CH2原子团,因而它们互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸丁酯的实验装置有以下甲、乙两种装置可供选用。

制备乙酸丁酯所涉及的有关物质的物理性质见下表:
乙酸 | 1-丁醇 | 乙酸丁酯 | |
熔点(℃) | 16.6 | -89.5 | -73.5 |
沸点(℃) | 117.9 | 117 | 126.3 |
密度(g/cm3) | 1.05 | 0.81 | 0.88 |
水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
(1)仪器M的名称为_________。
(2)制取乙酸丁酯选用乙装置而不选用甲装置的理由是__________。
(3)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是______(选填答案编号)。

(4)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须_____(填写操作)。某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能_________(写出一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列AI九种中学化学常见的物质之间的转化关系如图所示。已知A为固态非金属单质,B 在实验室常用作气体干燥剂,D为常见液体,常温下C、E、F都是无色气体,E能使酸性高锰酸钾溶液褪色,G是侯氏制碱法的最终产品
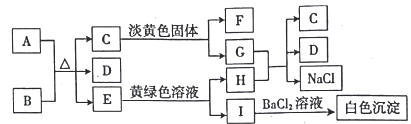
回答下列问题:
(1)F的分子式是________________,图中淡黄色固体中的阴、阳离子个数比为____________。
(2)A与B反应的化学方程式是:___________________________________________________。
(3)E转变为H和I的离子方程式是___________________________________________________。
(4)简述检验I溶于水电离所产生的阴离子的操作方法、实验现象和结论: ____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com