
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42﹣、NO3﹣、Cl﹣,该溶液放在用惰性材料做电极的电解槽中,通电片刻后,则氧化产物与还原产物的质量之比为()
A. 35.5:108 B. 16:207 C. 8:1 D. 108:35.5
考点: 电解原理.
专题: 电化学专题.
分析: 等物质的量的这些离子加入到水中,Ag+和Cl﹣沉淀为AgCl,Pb 2+ 和SO4 2﹣沉淀为PbSO4,
溶液中就只有Na+、NO3﹣了,实际上的电解NaNO3溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气.
解答: 解:等物质的量的这些离子加入到水中,Ag+和Cl﹣沉淀为AgCl,Pb 2+ 和SO4 2﹣沉淀为PbSO4,
溶液中就只有Na+、NO3﹣了,实际上是电解NaNO3溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气,当转移相同电子时,氧化产物和还原产物的质量之比为32:(2×2)=8:1,
故选C.
点评: 本题考查了离子共存和电解池原理,明确实际上电解的物质是解本题关键,很多同学忘记部分离子不能共存而导致错误,属于易错题.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
常温下,一定浓度的某溶液,由水电离出的c(OH﹣﹣)=10﹣﹣4mol/L,则该溶液中的溶质可能是()
A. Na2SO4 B. CH3COOH C. NaOH D. CH3COOK
查看答案和解析>>
科目:高中化学 来源: 题型:
A元素得电子变成阴离子时放出的能量比B元素得电子成阴离子时放出的能量大,那么下列判断正确的是()
A. 氧化性A﹣>B﹣ B. 还原性A﹣>B﹣ C. 氧化性A>B D. 还原性A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
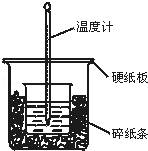
50mL 0.50mol•L﹣1盐酸与50mL 0.55mol•L﹣1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)烧杯间填满碎纸条的作用是 .
(2)大烧杯上如不盖硬纸板,求得的中和热的数值 (填“偏大”“偏小”“无影响”).
(3)从实验装置上看,图中尚缺少环形玻璃搅拌棒,如此求得的中和热的数值 (填“偏大”“偏小”“无影响”).
(4)实验中改用60mL 0.50mol•L﹣1盐酸跟50mL 0.55mol•L﹣1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热相等(填“相等”“不相等”),简述理由: .
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 ;用50mL 0.50mol•L﹣1NaOH溶液进行上述实验,测得的中和热的数值会 .(均填“偏大”“偏小”“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为()
A. 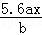 B.
B. 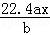 C.
C. 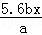 D.
D. 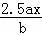
查看答案和解析>>
科目:高中化学 来源: 题型:
按图的装置进行电解,A极是铜锌含金,B极为纯铜.电解质溶液中含有足量的Cu2+.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A极合金中Cu、Zn的原子个数比为()
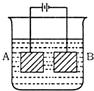
A. 4:1 B. 3:1 C. 2:1 D. 5:3
查看答案和解析>>
科目:高中化学 来源: 题型:
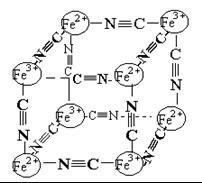
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
A.该晶体是原子晶体
B.M的离子位于上述立方体的面心,呈+2价
C.M的离子位于上述立方体的体心,呈+1价,且M+空缺率(体心中没有M+的占总体心的百分比)为50%
D.晶体的化学式可表示为MFe2(CN)3,且M为+1价
查看答案和解析>>
科目:高中化学 来源: 题型:
盐类水解程度的大小可以用”水解度”来表示。关于NaA(A-表示一元酸根离子)型盐的水解度,就是已水解的盐的物质的量占原来盐总物质的量的百分数。若测得2 L 0.1 mol • L﹣1的强碱弱酸盐NaA溶液的pH为10,则A-的水解度是
| A.0.01% | B.0.1% | C.0.2% | D.l% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com