
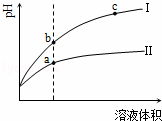
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
|
| A. | Ⅱ为盐酸稀释时的pH值变化曲线 |
|
| B. | b点溶液的导电性比c点溶液的导电性强 |
|
| C. | a点Kw的数值比c点Kw的数值大 |
|
| D. | b点酸的总浓度大于a点酸的总浓度 |
考点:
比较强弱电解质的实验.
专题:
压轴题.
分析:
根据盐酸是强酸,完全电离,醋酸是弱酸,部分电离,相同温度下,相同pH值的盐酸和醋酸溶液,醋酸浓度大,溶液稀释时,醋酸进一步电离,其溶液中离子浓度大于盐酸的离子浓度,故II应为醋酸稀释时的pH值变化曲线,利用c点、b点溶液中的离子浓度来分析导电性;Kw只与温度有关,与溶液的种类以及浓度大小没有关系;相同pH值的盐酸和醋酸,稀释到相同体积时,醋酸(II)浓度大于盐酸(I)浓度.
解答:
解:A、Ⅱ应为醋酸稀释时的pH值变化曲线,故A错;
B、溶液导电性取决于离子浓度,b点的H+浓度大,导电性强,故B正确;
C、Kw的大小只取决于温度,故C错;
D、相同pH值的盐酸和醋酸,醋酸浓度远大于盐酸的浓度,稀释到相同体积时,醋酸(Ⅱ)浓度大于盐酸(Ⅰ)浓度,故D错.
故选B.
点评:
本题考查强弱电解质溶液稀释时的浓度变化,注意加水促进弱电解质电离的特点.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
(1)在100℃时,PH=7呈 性.
(2)碳酸钠溶液呈碱性的原因,用离子方程式表示: .
(3)氯化铝溶液呈酸性的原因,用离子方程式表示:
(4)写电离方程式NaHCO3
(5)由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
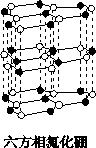
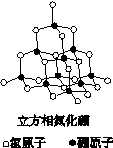
关于这两种晶体的说法,正确的是
| A.立方相氮化硼含有σ键和π键,所以硬度大 | B.六方相氮化硼层间作用力小,所以质地软 |
| C.两种晶体中的既有极性键又有非极性键 | D.两种晶体均为原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂。试回答下列问题:
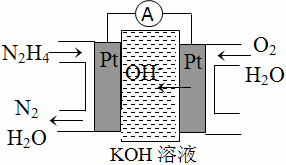
(1)肼燃料电池原理如图所示,左边电极上发生的电极反应式为____________________________________。
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
N2(g)+2O2(g) 2NO2(g) ΔH=-67.7kJ·mol-1
2NO2(g) ΔH=-67.7kJ·mol-1
N2H4(g)+O2(g) N2(g)+2H2O(g) ΔH=-534.0kJ·mol-1
N2(g)+2H2O(g) ΔH=-534.0kJ·mol-1
2NO2(g) N2O4(g) ΔH=-52.7kJ·mol-1
N2O4(g) ΔH=-52.7kJ·mol-1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:________________________________________________________________。
(3)联氨的工业生产常用氨和次氯酸钠为原料获得,也可在高锰酸钾催化下,尿素[CO(NH2)2]和次氯酸钠—氢氧化钠溶液反应获得,尿素法反应的离子方程式为_____________________________________________________。
(4)如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L。
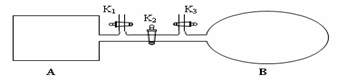
①B中可通过__________________________判断可逆反应2NO2 N2O4已经达到平衡。
N2O4已经达到平衡。
②若平衡后在A容器中再充入0.5mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数________(填 “变大”、“变小”或“不变”)
③若容器A中到达平衡所需时间t s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)等于____________________。
④若打开K2,平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是( )
|
| A. | 用10mL量筒量取7.13mL稀盐酸 |
|
| B. | 用托盘天平称量25.20g NaCl |
|
| C. | 用广泛pH试纸测得某溶液的pH为2.3 |
|
| D. | 用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知当NH4Cl溶液的浓度小于0.1mol/L时,其pH>5.1.现用0.1mol/L的盐酸滴定10mL0.05mol/L的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是( )
|
| A. | 10mL | B. | 5mL | C. | 大于5mL | D. | 小于5mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中,正确的是( )
|
| A. | 乙烯、苯、乙醇均能使紫色的酸性高锰酸钾溶液褪色 |
|
| B. | 乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 |
|
| C. | 油脂在碱的作用下可发生水解,工业上利用该反应生产肥皂 |
|
| D. | 乙酸乙酯、油脂、果糖、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明苯环对甲基有影响的是( )
|
| A. | 甲苯与氢气加成 |
|
| B. | 甲苯与硝酸浓硫酸作用制三硝基甲苯 |
|
| C. | 甲苯能使KMnO4酸性溶液褪色而乙烷不能 |
|
| D. | 苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com