
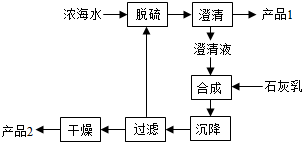
| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g?L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
| 1 |
| 1+5 |
| 5 |
| 3 |
| 5 |
| 3 |
| 58g |
| 24g |
| ||
| ||
| ||
| ||


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д� ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����AgNO3��Һ�еμӰ�ˮ��������Ag++NH3?H2O�TAgOH��+NH4+ |
| B����Mg��OH��2����Һ�еμ�FeCl3��Һ��3Mg��OH��2+2Fe3+�T2Fe��OH��3+3Mg2+ |
| C����Na2S2O3��Һ�м�������ϡ���2S2O32-+4H+�TSO42-+3S��+2H2O |
D��������Һ��ͨ������CO2���壺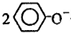 +CO2+H2O��2 +CO2+H2O��2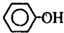 +CO32- +CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ӦA2��g��+3B2��g���T2AB3��g����һ���¶������Է����У���÷�Ӧ�ġ�H��0 |
| B����NH3 ͨ���ȵ�CuSO4 ��Һ����ʹCu2+��ԭ��Cu |
| C���ƺ�þ���Ȼ�����Һ�����ᾧ�����Ĺ��嶼��ˮ��������յ���Ӧ��ˮ�� |
| D�������ܽ������ʱ���ܽ�����������Ĵ����йأ�����Խ������Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
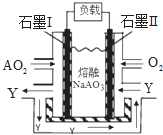 A��B��C��D��EΪԭ���������������Ԫ�أ�����ֻ��E�����ڶ����ڣ������Ϣ���±���
A��B��C��D��EΪԭ���������������Ԫ�أ�����ֻ��E�����ڶ����ڣ������Ϣ���±���| Ԫ�� | A | B | C | D | E |
| ��� ��Ϣ |
�������������۴�����Ϊ2 | ��Ԫ��C���γ����Ӹ�����Ϊ2��1��1��1�Ļ����� | ����������ͨ��������ú���� | DԪ�ؿ��γ��������������һ�����γ��������Ҫ�ɷ� | �䵥������;��㷺�Ľ���������ȱ�ٸ�Ԫ����ƶѪ֢ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
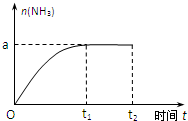 ��֪N2��g��+3H2��g��?2NH3��g������H=-92.4kJ?mol-1��
��֪N2��g��+3H2��g��?2NH3��g������H=-92.4kJ?mol-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 25��ʱ�������ᣨHA�������Σ�NaA����ɵĻ����Һ����ʼŨ�Ⱦ�Ϊ1mol?L-1����ͼΪ�����Һ��ͨ��HCl��������NaOH����ʱ����ҺpH�����H+��OH-�����ʵ������仯�����ߣ�����˵���У���ȷ���ǣ�������
25��ʱ�������ᣨHA�������Σ�NaA����ɵĻ����Һ����ʼŨ�Ⱦ�Ϊ1mol?L-1����ͼΪ�����Һ��ͨ��HCl��������NaOH����ʱ����ҺpH�����H+��OH-�����ʵ������仯�����ߣ�����˵���У���ȷ���ǣ�������| A����NaOH��HA����ƽ�ⳣ������ |
| B��ͨ��HCl����Һ��������Ũ��֮�ͼ�С |
| C����Һ��ˮ�ĵ���̶�a��b��c |
| D��b����Һ�У�c��HA����c��A-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
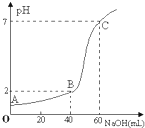 �����£�ȡ20mLijŨ�ȵ�HCl��Ϊ����Һ����һ�����ʵ���Ũ�ȵ�NaOH��Һ���еζ�������������NaOH��Һ��Ϻ�����仯���Բ��ƣ����ζ���������Һ��pH�仯����ͼ��ʾ������������ȷ���ǣ�������
�����£�ȡ20mLijŨ�ȵ�HCl��Ϊ����Һ����һ�����ʵ���Ũ�ȵ�NaOH��Һ���еζ�������������NaOH��Һ��Ϻ�����仯���Բ��ƣ����ζ���������Һ��pH�仯����ͼ��ʾ������������ȷ���ǣ�������| A������HCl��Ũ����0.09mol?L-1��NaOH��ҺŨ��Ϊ0.03mol?L-1 |
| B����B�㣬��Һ������Ũ�ȹ�ϵΪ��c��Cl-����c��Na+����c��H+����c��OH-�� |
| C��A��B��C����ˮ�ĵ���̶ȴ�С����Ϊ��A��B��C |
| D���ζ�ǰ����ƿ�ô���Һ��ϴ������HClŨ��ƫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
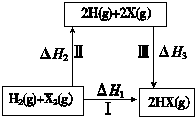 ������ͼ��ʾת����ϵ��X����±�أ���˵������ȷ���ǣ�������
������ͼ��ʾת����ϵ��X����±�أ���˵������ȷ���ǣ�������| A��2H��g��+2X��g���T2HX��g����H3��0 |
| B��;��������HX�ķ�Ӧ����;���أ����ԡ�H1=��H2+��H3 |
| C��Cl��Br��I�ķǽ��������μ���������;�������յ������������� |
| D��;��������HCl�ų�������������HBr�Ķ࣬˵��HCl��HBr�ȶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com