
(14分)(1)Na2SO3溶液蒸干得到的固体物质是___________,原因是______________.
(2)碳酸氢钡溶液蒸干得到的固体物质是___________,原因是___________________.
(3)盐酸与硫酸浓度各为1mol/L 的混合酸10mL,加热浓缩至1mL,最后得到的溶液浓度
为_________,原因是_____________________________________________________。
(4)与c(H+)·c(OH-)=kw类似,FeS饱和溶液中存在:FeS(s)  Fe
Fe
 +S
+S
 ,
,
c(Fe )·c(s
)·c(s )=ksp。常温下ksp=8.1×10-17。(溶液密度为1.0g/cm3)。
)=ksp。常温下ksp=8.1×10-17。(溶液密度为1.0g/cm3)。
理论上FeS的溶解度为___________________。
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
(每空2分,共14分)A、B、C、D均为含苯环的化合物,且相对分子质量B>A>C,已知有机物A的结构简式为: 
(1)A既能和NaOH溶液反应,又能和NaHCO3溶液反应,写出A和 NaHCO3溶液反应的化学方程式______ __________。
(2)①有机物B在浓硫酸存在条件下,相互作用生成一种环状酯(如下图)则有机物B的结构简式为 _。
②等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为___ _____。
(3) 1molA、C完全燃烧,消耗O2的质量相等,且1molC能和1molNa完全反应,写出含碳原子数最少的C的结构简式_____ ___,写出C与浓溴水的反应的化学方程式 。
(4)D和B互为同分异构体,且知其苯环上连有三个取代基,苯环上的一氯代物只有两种,D不与NaHCO3溶液反应,能与Na和NaOH反应,等质量的D消耗Na和NaOH的物质的量之比为2∶3,则D的结构简式为 、 。(只写二种)
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)(1)448mL某气体在标准状况下的质量为1.28g,该气体的摩尔质量约为
(2)12.4gNa2R中含Na+0.4mol,则Na2R的摩尔质量为 ,R的相对原子质量为
(3)5molCO2的质量是_________;在标准状况下所占的体积约为__________;所含的分子数目约为____________________;所含氧原子的数目约为___________________。
查看答案和解析>>
科目:高中化学 来源:2012届云南省建水一中高三9月份月考理科综合试题(化学部分) 题型:填空题
(14分)
Ⅰ.(每空1分) 已知某工业废水中含有大量的CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其他物质。
(1)步骤1需用到的玻璃仪器除烧杯外有 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式) ,固体残渣的成分是(填化学式) 。
(3)步骤3中涉及的操作是:蒸发浓缩、 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是 。
Ⅱ.((2)为1分,其余每空2分)某溶液中含有Na+、SO、SO、CO、Cl-、Br-中的若干种,依次进行下列实验,观察到的现象记录如下:①加入盐酸,有无色气体生成;②向原溶液中滴加氯水,无气体产生,再加CCl4振荡,静置,CCl4层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入Ba(NO3)2和HNO3的混合溶液,有白色沉淀生成,过滤;④在滤液中加AgNO3和HNO3的混合液,有白色沉淀产生.试回答:(提示:氯气会氧化SO为SO)
(1)原溶液中肯定存在的离子是 ,肯定没有的离子是 ;
(2)若步骤③改用BaCl2和盐酸的混合溶液,对判断(1)结论有无影响 ;
(3)步骤②中发生反应的离子方程式为 、 .
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省长安一中高一上学期期中考试化学试卷 题型:填空题
(14分)(I)下列离子均为中学化学常见的离子:Na+、Ba2+、Mg2+、Al3+、Fe3+、Cu2+、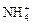 、H+、Cl-、
、H+、Cl-、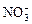 、
、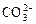 、
、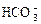 、
、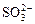 、OH-。上述离子中,在强酸性溶液里不可能大量存在的是____________;在强碱性溶液中不可能大量存在的离子有____________;既不能在强酸性溶液里大量存在,也不能在强碱性溶液里大量存在的是______;无论在强酸性溶液还是强碱性溶液里,都可以大量存在的是____________
、OH-。上述离子中,在强酸性溶液里不可能大量存在的是____________;在强碱性溶液中不可能大量存在的离子有____________;既不能在强酸性溶液里大量存在,也不能在强碱性溶液里大量存在的是______;无论在强酸性溶液还是强碱性溶液里,都可以大量存在的是____________
(II)将适当的物质填在下边的横线上
(1)Cu2++______=Fe2++______;
(2) ______+H+=______+H2O+CO2↑;
(3) 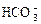 +______=
+______=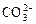 +______;
+______;
查看答案和解析>>
科目:高中化学 来源:2011-2012学年云南省高三9月份月考理科综合试题(化学部分) 题型:填空题
(14分)
Ⅰ.(每空1分) 已知某工业废水中含有大量的CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其他物质。

(1)步骤1需用到的玻璃仪器除烧杯外有 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式) ,固体残渣的成分是(填化学式) 。
(3)步骤3中涉及的操作是:蒸发浓缩、 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是 。
Ⅱ.((2)为1分,其余每空2分)某溶液中含有Na+、SO、SO、CO、Cl-、Br-中的若干种,依次进行下列实验,观察到的现象记录如下:①加入盐酸,有无色气体生成;②向原溶液中滴加氯水,无气体产生,再加CCl4振荡,静置,CCl4层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入Ba(NO3)2和HNO3的混合溶液,有白色沉淀生成,过滤;④在滤液中加AgNO3和HNO3的混合液,有白色沉淀产生.试回答:(提示:氯气会氧化SO为SO)
(1)原溶液中肯定存在的离子是 ,肯定没有的离子是 ;
(2)若步骤③改用BaCl2和盐酸的混合溶液,对判断(1)结论有无影响 ;
(3)步骤②中发生反应的离子方程式为 、 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com