
 储氢材料的种类很多,包括储氢合金、配位氢化物、碳质吸附材料等.
储氢材料的种类很多,包括储氢合金、配位氢化物、碳质吸附材料等.分析 (1)①Fe是26号元素,价电子数为8,根据原子核外电子排布规律排布;
②Ti是22号元素,原子核外有spd等能级;
(2)同周期随原子序数增大,第一电离能呈增大趋势,元素原子各轨道为半满、全满、全空时,能量较低,第一电离能高于同周期相邻元素的;
(3)根据价层电子对互斥理论确定空间构型;
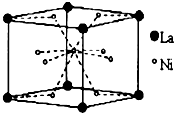
(4)①根据均摊法计算出晶胞中各原子的个数,再确定化学式;
②根据V=$\frac{m}{ρ}$计算出晶胞的体积,进而计算出晶胞的边长,根据晶胞图可知,两个距离最近的La原子间的距离为晶胞的边长.
解答 解:(1)①Fe是26号元素,位于元素周期表中第四周期第ⅥB族,故Ti的基态原子价电子排布式为 3d64s2,故答案为:3d64s2;
②Ti是22号元素,原子核外有1s、2s、3s、4s、2p、3p、3d等7个能级,故答案为:7;
(2)同周期随原子序数增大,第一电离能呈增大趋势,Mg元素原子2s轨道为全满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:Mg>Al>Na,
故答案为:Mg>Al>Na;
(3)AlH4-中Al原子价层电子对=4+$\frac{1}{2}$(3+1-4)=4,且没有孤电子对,所以是正四面体结构,故答案为:正四面体;
(4)①根据均摊法可知,晶胞中La原子的个数为$8×\frac{1}{8}$=1,Ni原子个数为$8×\frac{1}{2}+1$=5,所化学式为LaNi5,
故答案为:LaNi5;
②根据V=$\frac{m}{ρ}$计算出晶胞的体积为$\frac{M}{a{N}_{A}}$cm3,所以晶胞的边长为$\root{3}{\frac{M}{a{N}_{A}}}$cm,根据晶胞图可知,两个距离最近的La原子间的距离为晶胞的边长,所以两个距离最近的La原子间的距离为$\root{3}{\frac{M}{a{N}_{A}}}$cm,
故答案为:$\root{3}{\frac{M}{a{N}_{A}}}$cm.
点评 本题考查物质结构和性质,涉及核外电子排布、空间构型的判断、晶胞的计算等知识点,难点是晶胞的计算,灵活运用公式是解本题关键,难度中等.


科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 甲烷 | 一氧化碳 | 乙烯 | 苯 | 甲苯 | 苯酚 | 氨水 |

 、
、 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
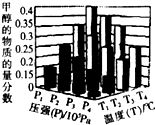 反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,
反应3H2(g)+CO2(g)?CH3OH(g)+H20(g)△H<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,| A. | P3>P2,T3>T2 | B. | P2>P4,T4>T2 | C. | P1>P3,T1>T3 | D. | P1>P4 T2<T3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
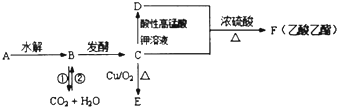
 外,还含有的官能团名称是碳碳双键和酯基;
外,还含有的官能团名称是碳碳双键和酯基; .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和溴用铁作催化剂生成溴苯 | |
| B. | 向苯酚浓溶液中滴入少量浓溴水可观察到白色三溴苯酚沉淀 | |
| C. | 氯乙烷与NaOH溶液共热,在水解后的溶液中加入硝酸酸化的AgNO3溶液检验Cl- | |
| D. | 向淀粉在酸性条件下水解的产物中加银氨溶液,水浴加热,检验葡萄糖的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食用植物油水解均可生成甘油 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 苯和浓硝酸反应生成硝基苯,乙酸和乙醇反应生成乙酸乙酯,二者反应类型相同 | |
| D. | 向蔗糖水解后的溶液中加新制的Cu(OH)2悬浊液,加热到沸腾即可验证水解产物葡萄糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com