
����Ŀ�����ʵ����ڼ����е�Ӧ��
��1���е�������������O3�� O2 ��ͬ��ͬѹ�µ��ܶ�֮��Ϊ______��
��2����7.8gNa2R��Na+Ϊ0.2mol����Na2R��Ħ������Ϊ_____��R�����ԭ������Ϊ___��
��3��������Ϊ51��32��34��NH3��CH4��H2S�������ʵ���֮��Ϊ___������������ԭ����֮��Ϊ__������������֮��Ϊ___��
��4����150��C��m gNH4HCO3������ȫ�ֽ�����NH3��CO2��H2O�������û�������H2������ܶ�Ϊd�����ú�m��d�Ĵ���ʽ��ʾ�����������ʵ���Ϊ_________��
��5��ij�����������������Ϊ36.5%���ܶ�Ϊ1.18g/cm3,����������ʵ���Ũ��Ϊ_______��
���𰸡�3��2 62g/mol 32 3:2:1 12:10:3 15:10:9 ![]() mol 11.8 mol/L
mol 11.8 mol/L
��������
��1��ͬ��ͬѹ�����ʵ��ܶ�֮�ȵ���Ħ������֮�ȣ����������O3�� O2ͬ��ͬѹ�µ��ܶ�֮��Ϊ48g/mol�� 32g/mol=3��2���ʴ�Ϊ��3��2��
��2��7.8gNa2R��Na+Ϊ0.2mol����Na2R��Ħ������Ϊ![]() =78g/mol����Na2X����Է�������Ϊ78��֪��X�����ԭ������Ϊ��78��23��2��=32���ʴ�Ϊ��62g/mol��32��
=78g/mol����Na2X����Է�������Ϊ78��֪��X�����ԭ������Ϊ��78��23��2��=32���ʴ�Ϊ��62g/mol��32��
��3��������Ϊ51��32��34��NH3��CH4��H2S�����ʵ���֮��Ϊ![]() ��
��![]() ��
��![]() =3:2:1��������ԭ����֮��Ϊ3��4:2��5:1��3=12:10:3������������֮��Ϊ3��10:2��10:1��18=15:10:9���ʴ�Ϊ��3:2:1��12:10:3��15:10:9��
=3:2:1��������ԭ����֮��Ϊ3��4:2��5:1��3=12:10:3������������֮��Ϊ3��10:2��10:1��18=15:10:9���ʴ�Ϊ��3:2:1��12:10:3��15:10:9��
��4��150��Cʱ̼��������ȷֽ����ɰ�����������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪNH4CO3![]() NH3����CO2����H2O���������غ㶨�ɿ�֪��������������Ϊmg���ɻ�������H2������ܶ�Ϊd��֪����������Ħ������Ϊ2dmol/L��������������ʵ���Ϊ
NH3����CO2����H2O���������غ㶨�ɿ�֪��������������Ϊmg���ɻ�������H2������ܶ�Ϊd��֪����������Ħ������Ϊ2dmol/L��������������ʵ���Ϊ![]() =
=![]() mol���ʴ�Ϊ��
mol���ʴ�Ϊ��![]() mol��
mol��
��5�������ʵ���Ũ�Ⱥ����������Ĺ�ϵʽc=![]() ��֪����������36.5%���ܶ�1.18g/mLŨ��������ʵ���Ũ��c=
��֪����������36.5%���ܶ�1.18g/mLŨ��������ʵ���Ũ��c=![]() mol/L=11.8 mol/L���ʴ�Ϊ��11.8 mol/L��
mol/L=11.8 mol/L���ʴ�Ϊ��11.8 mol/L��


 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��Ӧ��:Fe(s)+CO2(g)![]() FeO(s)+CO(g),�仯ѧƽ�ⳣ��ΪK1;��ѧ��Ӧ��:Fe(s)+H2O(g)
FeO(s)+CO(g),�仯ѧƽ�ⳣ��ΪK1;��ѧ��Ӧ��:Fe(s)+H2O(g)![]() FeO(s)+H2(g),�仯ѧƽ�ⳣ��ΪK2,���¶�973 K��1173 K�������,K1��K2��ֵ�ֱ�����:
FeO(s)+H2(g),�仯ѧƽ�ⳣ��ΪK2,���¶�973 K��1173 K�������,K1��K2��ֵ�ֱ�����:
�¶� | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)ͨ�������е���ֵ�����ƶ�:��Ӧ����_______(��������������������)��Ӧ��
(2)���з�Ӧ��:CO2(g)+H2(g)![]() CO(g)+H2O(g),����д���÷�Ӧ��ƽ�ⳣ��K3�ı���ʽ:K3=______��
CO(g)+H2O(g),����д���÷�Ӧ��ƽ�ⳣ��K3�ı���ʽ:K3=______��
(3)���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵʽΪ__________,�ݴ˹�ϵʽ���ϱ�����,���ƶϳ���Ӧ����________(��������������������)��Ӧ��
(4)Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ�,�ɲ�ȡ�Ĵ�ʩ��______ ��_____ (��д��ĸ���)��
A.��С��Ӧ�������ݻ� B.����Ӧ�������ݻ�
C.�����¶� D.ʹ�ú��ʵĴ���
E.�跨��Сƽ����ϵ�е�CO��Ũ��
(5)ͼ�ס��ҷֱ��ʾ��Ӧ����t1ʱ�̴ﵽƽ��,��t2ʱ����ı�ij�������������仯�����:

��ͼ����t2ʱ�̷����ı��������__________��
��ͼ����t2ʱ�̷����ı��������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019���������ʻ�ѧԪ�����ڱ������������й�˵������ȷ����
A. ��������ﰺ-12(CCl2F2)���з����ã����������Ԫ�����ڱ���ָ������
B. ͨ���ⶨ������![]() �ĺ��������ƶ���������
�ĺ��������ƶ���������
C. �Ž��з�Ԥ�Ե��������� ��(Ga)Ԫ�صķ��֣�֤ʵ��Ԫ�������ɵĿ�ѧ��
D. ����Ԫ��Ti��Mo��W�ȵĵ��������£���ʴ���ص㣬��Ͻ����������������������ɴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������ºϳ���ϩ��6H2(g)��2CO2(g)![]() CH2��CH2(g)��4H2O(g)����֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵������ȷ���ǣ� ��
CH2��CH2(g)��4H2O(g)����֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵������ȷ���ǣ� ��

A. ������ϩ�����ʣ�v(N)һ������v(M) B. �÷�Ӧ���淴ӦΪ���ȷ�Ӧ
C. ƽ�ⳣ����KM��KN D. ���¶ȸ���250 �棬�����¶ȣ������Ĵ�Ч�ʽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ļ������ڹ�ũҵ�����������о�����ҪӦ�á���ش�����������
(1)���������г���N2H4��Ϊ����������ȼ����N2H4�백�����ƣ���һ�ּ������壬������ˮ����������N2H4��H2O���õ��뷽��ʽ��ʾN2H4��H2O�Լ��Ե�ԭ�� ��
��2���ں��������£�1 mol NO2������C������Ӧ:2NO2(g)+2C(s)![]() N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) Kc(B)�������������=������
��A��B��C������NO2��ת������ߵ��� ������A������B������C��������
������C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp= ���г�����ʽ����������Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�����������
��3��������ĵ���ƽ�ⳣ��Ka=5.1��10-4��298K�����������ʺ���������ơ�
����֪298K ʱ��H2CO��Ka1=4.2��10-7 ��Ka2=5.61��10-11������2mol̼���Ƶ���Һ�м���1mol��HNO2������Һ��CO32-��HCO3-��NO2-������Ũ���ɴ�С�� ��
����10mL0.1mol/L����������Һ���뵽10mL0.1mol/L��ˮ����֪��25��ʱ��һˮ�ϰ���Ki= 1.8��10-5����,���������ҺΪ________��������������������������������������
��4��һ��ú̿������������Ԫ����CaSO4���γɹ̶���������������CO�ֻ���CaSO4������ѧ��Ӧ����ص��Ȼ�ѧ����ʽ���£�
��CaSO4��s��+CO��g��![]() CaO��s��+SO2��g��+CO2��g����H = +210.5kJmol-1
CaO��s��+SO2��g��+CO2��g����H = +210.5kJmol-1
��CaSO4��s��+ 4CO��g��![]() CaS��s��+ 4CO2��g�� ��H = -189.2kJmol-1
CaS��s��+ 4CO2��g�� ��H = -189.2kJmol-1
��ӦCaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) ��H= kJmol-1��
CaS(s)+3CO2(g) ��H= kJmol-1��
(5)H2S��������ˮ�γɵ���������һ�ֶ�Ԫ���ᣬ25��ʱ����0.10 mol��L-1H2S��Һ�У�ͨ��HCl��������NaOH�����Ե�����ҺpH����ҺpH��c(S2-)��ϵ��ͼ��ʾ(������Һ����ı仯��H2S�Ļӷ�)��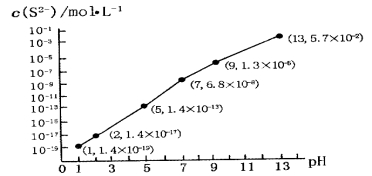
��pH=13ʱ����Һ�е�c(H2S)+c(HS-)=__________mol��L-1��
��ij��Һ��0.010 mol��L-1Fe2+��0.10 mol��L-1H2S������ҺpH=______ʱ��Fe2+��ʼ����������֪��KSP(FeS)=1.4��10-19��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ŀ���������ù����ռ���Һ����ij����(��Al2O3��MgO)�����˺�õ���Һ��NaHCO3��Һ�����������ҺpH��Al(OH)3���ɵ��������NaHCO3��Һ����仯����������:

�����й�˵������ȷ����
A. ԭNaHCO3��Һ��c(H2CO3)+c(HCO3-)+c(CO32-)=0.8moL/L
B. a��ˮ�ĵ���̶�С��c��ˮ�ĵ���̶�
C. a����Һ�д���:c(Na+)+c(H+)=c(AlO2-)+(OH-)
D. ���ɳ��������ӷ���ʽΪ��HCO3-+AlO2-+H2O=Al(OH)3��+CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������NaOH��������240mL 1.2mol/L��NaOH��Һ�������ش��������⣺
��1������240mL 1.2mol/L��NaOH��Һ
Ӧ��ȡNaOH������/g | ѡ������ƿ�Ĺ��/mL | ������ƿ���Ҫ�������������� |
_________ | ________ | _______ |
��2������ƿ����������������е�_____________________��
��Ũ�� �� �¶� ������ ��ѹǿ �ݿ̶���
��3������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ�___��
A��������ȴ��NaOH��Һ�ز�����ע��250mL������ƿ��
B������ƽȷ��ȡ�����NaOH����������������ˮ���ò���������������ʹ�����ܽ�
C����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
D��������ƿ�ǽ����ߵ�ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�������
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
G װ�����ñ�ǩ���Լ�ƿ����
��4���������Ƶ���ҺŨ��ƫ�͵���__��
A������NaOHʱ������ֽ�ϳ���
B������ǰ������ƿ������������ˮ
C��������ˮʱ���������˿̶���
D��������ƿ��ת����Һʱ������Һ����������ƿ����
E ����ƿ��ʹ��ǰ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������(ClCH2-COOH)���л��ϳ�����һ����Ҫ��ԭ�Ϻ��м��壬�����ʴ��¸������������ᷴӦ�Ƶ�һ�����![]()
![]()
![]()
��֪��

��ش��������⣺
(1)ѡ����ͼ��װ���Ʊ�һ�������Ʒ��

�ٰ����������������������ӵĺ���˳��Ϊ____��____��____��____��____��i��j��g��h����ӿ���ĸ����____
��ϴ��ƿ�е���ҺΪ____����ʯ�ҵ�������____��
(2)�Ʊ�һ������ʱ�����Ȳ���____������ˮԡ��������ԡ������ɳԡ�������ȷ��������¶���95�����ң����¶��ȶ����ٴ��ɼС�____��������������������ƿ��Һ����۲쵽���� ___��������ʱ��Ӧ��___������������Լ�������ͨ�����������˷ѡ�
(3)һ�������Ʒ�к��ж������ᡢ�������ᣬ���������Ʒ���Ժ���������____�����������ƣ����ٽ���____������������������Һ�������ؽᾧ�������ɵõ�������һ�����ᡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3��O2����ȼ�ϵ�ص�ʾ��ͼ���£��й�˵����ȷ����

A. a��ÿ����1molN2��Լ��6��6.02��1023��OH��Ǩ����b��
B. a���ĵ缫��ӦΪ��2NH3 ��6e�� = N2+ 6H+
C. b���ĵ缫��ӦΪ��4OH�� ��4e�� = 2H2O + O2��
D. �õ���ܷ�ӦΪ��4NH3 + 3O2 = 2N2 + 6H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com