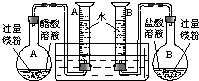
£Ø2009?ÕŲĒģ¶žÄ££©Ä³Š£æĘ¼¼»ī¶ÆŠ”×éÓĆĆ¾·Ū”¢ŃĪĖį”¢“×Ėį¼°Éč¼ĘµÄÓŅĶ¼×°ÖĆ£Ø¼Š³Ö¹Ģ¶Ø×°ÖĆŅŃĀŌČ„£©£¬¶ŌĮ½ÖÖĖį·Ö±šÓėĆ¾·“Ó¦µÄĖŁĀŹŅŌ¼°ŹĒ·ń“ęŌŚµēĄėĘ½ŗā½ųŠŠĢ½¾æ£®
£Ø1£©×é×°Ķź³Éŗó£¬Ä³Ķ¬Ń§·¢ĻÖøĆ×°ÖĆŌŚÉč¼ĘÉĻ“ęŌŚĆ÷ĻŌȱĻŻ£ŗøł±¾ĪŽ·ØĶź³ÉŹµŃ飬ÉõÖĮ“ęŌŚĪ£ĻÕ£¬ĘäȱĻŻŌŚÓŚ
A”¢BĮ½øöĮæĶ²æŚÓĆ½ŗČūĆÜ·ā£¬·“Ó¦²śÉśµÄH2»įŌģ³ÉŃ¹Ēæ¹ż“ó¶ų·¢ÉśĪ£ĻÕ[»ņĆÜ·āµÄĮæĶ²ÄŚĘųŃ¹Ėę·“Ó¦æŖŹ¼ŗ󲻶ĻŌö“󣬻įŌģ³ÉÉÕĘæ»ņĮæĶ²ŅņŃ¹Ēæ¹ż“󽫽ŗČūĶĘ³ö]
A”¢BĮ½øöĮæĶ²æŚÓĆ½ŗČūĆÜ·ā£¬·“Ó¦²śÉśµÄH2»įŌģ³ÉŃ¹Ēæ¹ż“ó¶ų·¢ÉśĪ£ĻÕ[»ņĆÜ·āµÄĮæĶ²ÄŚĘųŃ¹Ėę·“Ó¦æŖŹ¼ŗ󲻶ĻŌö“󣬻įŌģ³ÉÉÕĘæ»ņĮæĶ²ŅņŃ¹Ēæ¹ż“󽫽ŗČūĶĘ³ö]
£¬ĘäøĽų·½·ØŹĒ
³żČ„A”¢BĮæĶ²æŚµÄ½ŗČū
³żČ„A”¢BĮæĶ²æŚµÄ½ŗČū
£®
£Ø2£©øĽų×°ÖĆŗ󣬼ģ²éŅ»²ą×°ÖƵÄĘųĆÜŠŌµÄ·½·ØŹĒ
½«µ¼¹ÜæŚ·ÅČėĖ®²ŪÖŠ£¬ÓĆŹÖĪę×”ÉÕĘ棬Čē¹ūµ¼¹ÜæŚÓŠĘųÅŻ²śÉś£¬ĖÉæŖŹÖŗóµ¼¹ÜÄŚÓŠŅ»¶ĪĖ®Öł£¬Ö¤Ć÷×°ÖĆ²»Ā©Ęų
½«µ¼¹ÜæŚ·ÅČėĖ®²ŪÖŠ£¬ÓĆŹÖĪę×”ÉÕĘ棬Čē¹ūµ¼¹ÜæŚÓŠĘųÅŻ²śÉś£¬ĖÉæŖŹÖŗóµ¼¹ÜÄŚÓŠŅ»¶ĪĖ®Öł£¬Ö¤Ć÷×°ÖĆ²»Ā©Ęų
£®
£Ø3£©ÓūÅäÖĘ100mLŹµŃéĖłŠčÅØ¶ČµÄŃĪĖį£¬³ż50mLĮæĶ²”¢ÉÕ±”¢ĖįŹ½µĪ¶Ø¹Ü”¢½ŗĶ·µĪ¹ÜÖ®Ķā£¬»¹ŠčÓƵ½µÄÖ÷ŅŖ²£Į§ŅĒĘ÷ŹĒ
100mLČŻĮæĘ攢²£Į§°ō
100mLČŻĮæĘ攢²£Į§°ō
£®
ÕżČ·²Ł×÷£¬¼ĒĀ¼µĆµ½ĻĀ±ķÖŠ²æ·ÖŹµŃ鏿¾Ż£®·ÖĪöŹż¾Ż£¬¹Ū²ģŹµŃé×°ÖĆĶ¼£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
| AÉÕĘæÖŠ |
BÉÕĘæÖŠ |
20”ę”¢101kPa
50mLĮæĶ²ÄŚĘųĢå¶ĮŹż |
·“Ó¦Ź±¼ä |
| AĘæ |
BĘæ |
40mL0.1mol/L
“×ĖįČÜŅŗ |
40mL0.1mol/L
ŃĪĖįČÜŅŗ |
5mL |
t£Øa1£©=155s |
t£Øb1£©=7s |
| 10mL |
t£Øa2£©=310s |
t£Øb2£©=16s |
| 15mL |
t£Øa3£©=465s |
t£Øb3£©=30s |
| 20mL |
t£Øa4£©=565s |
t£Øb4£©=64s |
| ” |
” |
” |
| 44.8mL |
t£Øan£©=865s |
t£Øbn£©=464s |
£Ø4£©ŌŚŹµŃ鏿¾ŻÖŠ£ŗ¢Łt£Øa
1£©Ō¶Ō¶“óÓŚt£Øb
1£©µÄŌŅņĪŖ£ŗ
æŖŹ¼½×¶Ī“×ĖįČÜŅŗÖŠµÄ[H+]Ō¶Š”ÓŚĻąĶ¬ÅØ¶ČµÄŃĪĖįÖŠµÄ[H+]
æŖŹ¼½×¶Ī“×ĖįČÜŅŗÖŠµÄ[H+]Ō¶Š”ÓŚĻąĶ¬ÅØ¶ČµÄŃĪĖįÖŠµÄ[H+]
£»
¢ŚÓÉ
t£Øb3£©-t£Øb2£©£¾t£Øb2£©-t£Øb1£©»ņt£Øb3£©£¾t£Øb1£©+t£Øb2£©
t£Øb3£©-t£Øb2£©£¾t£Øb2£©-t£Øb1£©»ņt£Øb3£©£¾t£Øb1£©+t£Øb2£©
[ÓĆŗ¬t£Øb
1£©”¢t£Øb
2£©”¢t£Øb
3£©“śŹżŹ½±ķŹ¾]ĖµĆ÷ŃĪĖįŹĒæÉÄܲ»“ęŌŚµēĄėĘ½ŗā£»ÓÉ
t£Øa3£©-t£Øa2£©=t£Øa2£©-t£Øa1£©»ņt£Øa3£©=t£Øa1£©+t£Øa2£©
t£Øa3£©-t£Øa2£©=t£Øa2£©-t£Øa1£©»ņt£Øa3£©=t£Øa1£©+t£Øa2£©
[ÓĆŗ¬t£Øa
1£©”¢t£Øa
2£©”¢t£Øa
3£©“śŹżŹ½±ķŹ¾]ĖµĆ÷“×ĖįÖŠ“ęŌŚµēĄėĘ½ŗā£®
£Ø5£©ĶعżøĆŹµŃéæɵƵ½µÄ½įĀŪŹĒ£Ø»Ų“š³öĮ½µć¼“æÉ£©£ŗ¢Ł
ĻąĶ¬ĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖį”¢“×ĖįÓė½šŹō·“Ó¦Ź±£¬ŃĪĖįæŖŹ¼·“Ó¦ĖŁĀŹ“󣬹żŅ»¶ĪŹ±¼äŗó“×Ėį½ĻŃĪĖį·“Ó¦ĖŁĀŹµÄæģ
ĻąĶ¬ĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖį”¢“×ĖįÓė½šŹō·“Ó¦Ź±£¬ŃĪĖįæŖŹ¼·“Ó¦ĖŁĀŹ“󣬹żŅ»¶ĪŹ±¼äŗó“×Ėį½ĻŃĪĖį·“Ó¦ĖŁĀŹµÄæģ
£»¢Ś
ŃĪĖįŹĒĒæµē½āÖŹ£¬“×ĖįŹĒČõµē½āÖŹ£Ø“ęŌŚµēĄėĘ½ŗā£©
ŃĪĖįŹĒĒæµē½āÖŹ£¬“×ĖįŹĒČõµē½āÖŹ£Ø“ęŌŚµēĄėĘ½ŗā£©
£®





 £Ø2009?ÕŲĒģ¶žÄ££©Ä³Š£æĘ¼¼»ī¶ÆŠ”×éÓĆĆ¾·Ū”¢ŃĪĖį”¢“×Ėį¼°Éč¼ĘµÄÓŅĶ¼×°ÖĆ£Ø¼Š³Ö¹Ģ¶Ø×°ÖĆŅŃĀŌČ„£©£¬¶ŌĮ½ÖÖĖį·Ö±šÓėĆ¾·“Ó¦µÄĖŁĀŹŅŌ¼°ŹĒ·ń“ęŌŚµēĄėĘ½ŗā½ųŠŠĢ½¾æ£®
£Ø2009?ÕŲĒģ¶žÄ££©Ä³Š£æĘ¼¼»ī¶ÆŠ”×éÓĆĆ¾·Ū”¢ŃĪĖį”¢“×Ėį¼°Éč¼ĘµÄÓŅĶ¼×°ÖĆ£Ø¼Š³Ö¹Ģ¶Ø×°ÖĆŅŃĀŌČ„£©£¬¶ŌĮ½ÖÖĖį·Ö±šÓėĆ¾·“Ó¦µÄĖŁĀŹŅŌ¼°ŹĒ·ń“ęŌŚµēĄėĘ½ŗā½ųŠŠĢ½¾æ£®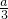 £©”Į22.4L£»
£©”Į22.4L£»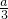 £©]mol£®
£©]mol£®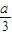 £©×22.4L£»
£©×22.4L£» £©]mol£®
£©]mol£®