
| A. | Zn为正极,Ag2O为负极 | |
| B. | Zn为负极,Ag2O为正极 | |
| C. | 原电池工作时,正极区溶液pH值减小 | |
| D. | 原电池工作时,负极区溶液pH值增大 |
分析 A、根据负极化合价升高失电子被氧化,正极化合价降低得电子发生还原反应判断;
B、根据负极化合价升高失电子被氧化,正极化合价降低得电子发生还原反应判断;
C、根据正极发生反应Ag2O+H2O+2e-=2Ag+2OH-,生成氢氧根离子判断该极区溶液PH值变化;
D、根据负极发生反应Zn+2OH--2e-═ZnO+H2O,消耗氢氧根离子判断该极区溶液PH值变化;
解答 解:A、Zn化合价升高失电子被氧化,应为原电池的负极,Ag2O化合价降低得电子发生还原反应,应为原电池的正极,故A错误;
B、Zn化合价升高失电子被氧化,应为原电池的负极,Ag2O化合价降低得电子发生还原反应,应为原电池的正极,故B正确;
C、原电池工作时,正发生反应Ag2O+H2O+2e-=2Ag+2OH-,该极区溶液PH值增大,故C错误;
D、原电池工作时,负发生反应Zn+2OH--2e-=ZnO+H2O,溶液PH值减小,故D错误.
故选B.
点评 本题考查原电池知识,题目难度不大,根据负极化合价升高失电子被氧化,正极化合价降低得电子发生还原反应判断.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
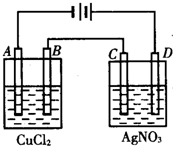 如图为以惰性电极进行电解:
如图为以惰性电极进行电解:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 2,3-二甲基-1-戊烯 | D. | 1,2,4-三甲基-1-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电子式: | |
| B. | 氮原子的L层电子轨道表示式: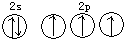 | |
| C. | 硫离子的核外电子排布式:1s22s22p63s23p4 | |
| D. | 碳-12原子:126C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 吸收塔中的硫元素可能以单质形式存在 | |
| B. | 中和池中只发生生成沉淀的复分解反应 | |
| C. | 在中和池中加入盐酸酸化的BaCl2溶液,可能产生白色沉淀 | |
| D. | 由题意分析得到,沉淀可能是Cr(OH)6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com