
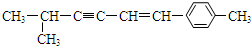 ,下列说法中正确的是( )
,下列说法中正确的是( )| A. | 该分子中所有的碳原子均可能处于同一平面上 | |
| B. | 该分子中一定共面的碳原子数至少为8个 | |
| C. | 该分子中至少有9个碳原子处于同一条直线上 | |
| D. | 该分子中可能共面的碳原子数最多为13个 |
分析 有机物中的原子共平面问题可以直接联想甲烷的正四面体结构、乙烯的平面型结构、乙炔的直线型结构和苯的平面型结构,对有机物进行肢解,分部分析,另外要重点掌握碳碳单键可旋转、双键和三键不可旋转,以此解答该题.
解答 解:A.此有机物中存在的C原子如图所示,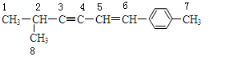 ,其中与2号碳相连的3和1、8这3个碳原子为四面体结构,不可能在同一平面上,故A错误;
,其中与2号碳相连的3和1、8这3个碳原子为四面体结构,不可能在同一平面上,故A错误;
B.该分子中,碳碳三键中的3、4号碳与双键中5、6号碳一定在同一平面上,与3号碳相连的2号碳一定在这个平面内,与6号碳相连的苯环上的碳以及其对面上的碳和7号碳一定在同一平面内,故最少在同一平面内的碳原子数是8,故B正确;
C.乙炔中所有原子共直线,故最多有4个原子在一条直线上,故C错误;
D.苯环、碳碳双键具有平面形结构,碳碳三键为直线形结构,与苯环、碳碳双键直接相连的原子可能在同一个平面上,最多有14个,包括2、3、4、5、6、7以及苯环的C原子,故D错误,
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重有机物的空间结构的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量 | B. | 原子数 | C. | 质子数 | D. | 密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子直径在1~100nm之间 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子能穿过滤纸 | D. | 胶体粒子能够发生布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图甲:进行中和热的测定 | |
| B. | 图乙:比较 HCl、H2CO3和 H2SiO3 的酸性强弱 | |
| C. | 图丙:验证 CuCl2对 H2O2 分解有催化作用 | |
| D. | 图丁:验证 2NO2(g)?N2O4(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
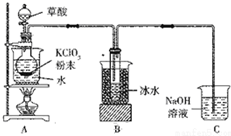 二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示:
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
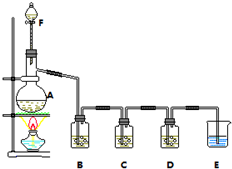 某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
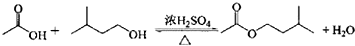
| 相对原子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.813 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
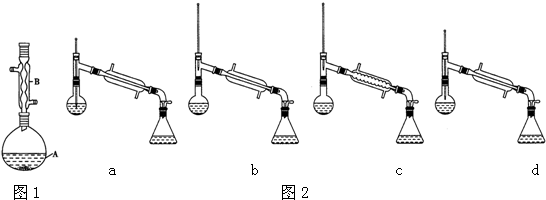
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com