
 (Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
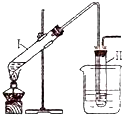 实验室用如图所示的装置制取溴乙烷.在试管Ⅰ中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管Ⅰ至微沸状态数分钟后,冷却.已知:通常情况下,溴乙烷呈液态,其密度比水大且不溶于水.试回答下列问题:
实验室用如图所示的装置制取溴乙烷.在试管Ⅰ中依次加入2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水.加热试管Ⅰ至微沸状态数分钟后,冷却.已知:通常情况下,溴乙烷呈液态,其密度比水大且不溶于水.试回答下列问题:| 实验步骤 | 实验操作 | 预期现象和结论 | ① | 取少量除杂后的溴乙烷于试管中, |
② | 取①中反应后的上层清液少量于另一支试管中, |
查看答案和解析>>
科目:高中化学 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:022
NO和NO2具有下列不同性质:(1)通常情况下,NO是无色气体,微溶于水;NO2是红棕色气体,易溶于水;(2)NO2与水反应为3NO2+H2O![]() 2HNO3+NO.如图,将一支充满NO2气体的试管倒立在烧杯中(水中已预先加入几滴石蕊试液),试分析反应完全后可能出现的实验现象________.
2HNO3+NO.如图,将一支充满NO2气体的试管倒立在烧杯中(水中已预先加入几滴石蕊试液),试分析反应完全后可能出现的实验现象________.

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
(1)O2和O3性质不同的原因是___________________________________________________。
(2)将带火星的木条伸入到盛有臭氧的集气瓶中,可以看到_____________现象。
(3)写出在臭氧发生器中O2转化成O3的化学方程式_______________________________。
(4)应采用什么方法保护臭氧层________________________________________________。
(5)SO2遇O3微热即被迅速氧化成SO3,SO3跟水反应生成硫酸,这是除去废气中SO2的理想方法。写出SO2与O3反应的化学方程式_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com