
【题目】(题文)一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO2![]() 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是
①相同时间内,氧气的生成速率为n mol·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
A. ①③⑤⑥ B. ②③⑤
C. ①③④ D. ①②③④⑤⑥
【答案】A
【解析】
(1)相同时间内, NO2的生成速率为2nmol·L-1·s-1,则氧气的反应速率是nmol·L-1·s-1,氧气的正逆反应速率相等。
(2) 单位时间内生成nmol 氧气的同时生成2nmol的一氧化氮,都代表正反应速率。
(3)混合气体的颜色不再改变,说明NO2气体的浓度不变。
(4)反应前后混合气体的质量不变且容器的体积不变,则密度始终不变。
(5)当达到平衡时,气体的物质的量不变,则混合气体的平均相对分子质量不再改变。
(6)反应前后气体的化学计量数之和不相等,当达到平衡时,气体的压强不变。
①相同时间内, NO2的生成速率为2nmol·L-1·s-1,则氧气的反应速率是nmol·L-1·s-1,根据已知条件知,氧气的正逆反应速率相等,所以该反应达到平衡状态,正确;②单位时间内生成nmol 氧气的同时生成2nmol的一氧化氮,反应同向,不能说明正逆反应速率相等,不能判断反应达到平衡状态,错误;混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,正确;④反应前后混合气体的质量不变且容器的体积不变,则密度始终不变,所以不能说明达到平衡状态,错误;⑤反应前后气体的化学计量数之和不相等,当达到平衡时,气体的物质的量不变,则混合气体的平均相对分子质量不再改变,正确;⑥反应前后气体的化学计量数之和不相等,当达到平衡时,气体的压强不变,正确;符合条件的有①③⑤⑥;正确选项A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】钒和镍及其化合物是重要合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的核外电子排布式为________,其排布时能量最高电子所占据能级的原子轨道有________个伸展方向。
(2)VO2+可与多种物质形成配合物,与氧同周期且第一电离能比氧大的主族元素有____(写元素符号)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______,与CN-互为等电子体的一种分子的化学式为__________。
(4)三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF3、H2O2等为主要原料来制取。
①H2O2分子中O原子的杂化方式为________。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为__________。
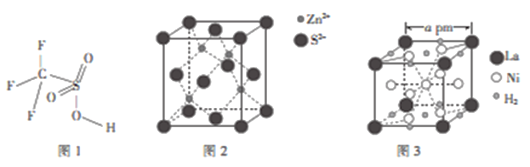
(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2所示,该晶胞中S2-的配位数为____。
(6)镧镍合金是重要储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为___________。
②该镧镍合金储氢后氢气的密度为________(用NA表示阿伏加德罗常数的数值)g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将pH=5的H2SO4的溶液稀释1000倍后,溶液中SO42-离子浓度与H+离子浓度的比值约为( )
A. 1∶1 B. 1∶2 C. 1∶10 D. 1∶20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)相同条件下,0.1molL﹣1的NH4Al(SO4)2中c(NH4+)(填“等于”、“大于”或“小于”)0.1molL﹣1NH4HSO4中c(NH4+).
(2)均为0.1molL﹣1的几种电解质溶液的pH随温度变化的曲线如图1所示. 
①其中符合0.1molL﹣1NH4Al(SO4)2的pH随温度变化的曲线是 , 导致pH随温度变化的原因是;
②20℃时,0.1molL﹣1的NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)=(取近似值)
(3)室温时,向100mL0.1molL﹣1NH4HSO4溶液中滴加0.1molL﹣1NaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图2所示: 试分析图中a、b、c、d四个点,水的电离程度最大的是点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个试管中,过氧化氢分解产生氧气的反应速率最快的是 ( )
试管 | 温度 | 过氧化氢溶液浓度 | 催化剂 |
A | 常温 | 3% | — |
B | 常温 | 6% | — |
C | 水浴加热 | 3% | — |
D | 水浴加热 | 6% | MnO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法不正确的是( )
A. 用报纸包装食物属于资源的充分利用,应以提倡。
B.  是矿泉水瓶、饮料瓶底的常见标志,表示可回收利用,只能一次性使用,不能长期使用。
是矿泉水瓶、饮料瓶底的常见标志,表示可回收利用,只能一次性使用,不能长期使用。
C. 具有吸水性的植物纤维加工后可用作食品干燥剂。
D. 防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25°时,乙酸和三氯乙酸的电离常数分别是:Ka(CH3COOH)═1.80×10﹣5 , Ka(CCl3COOH)═0.60,在物质的量浓度均为0.1molL﹣1的CH3COONa和CCl3COONa混合溶液中,下列关系正确的是( )
A.c(Na+)═c(CCl3COO﹣)+c(CH3COO﹣)
B.c(CCl3COO﹣)﹣c(CH3COO﹣)═c(CH3COOH)﹣c(CCl3COOH)
C.c(OH﹣)>c(CCl3COO﹣)>c(CH3COO﹣)
D.c(CH3COOH)>c(CCl3COOH)>c(OH﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com