
| A、苯酚和甲醛在一定条件下可合成酚醛树脂 |
B、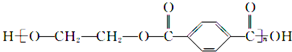 的单体是HOCH2CH2OH与 的单体是HOCH2CH2OH与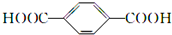 |
| C、聚苯乙烯是由苯乙烯加聚生成的纯净物 |
D、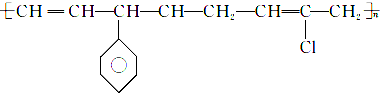 的单体有3种 的单体有3种 |
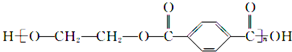 中含-COOC-及端基原子和原子团,为缩聚产物;
中含-COOC-及端基原子和原子团,为缩聚产物;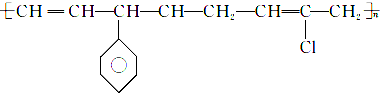 中主链只含C,为加聚反应产物.
中主链只含C,为加聚反应产物.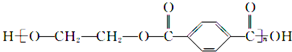 中含-COOC-及端基原子和原子团,为缩聚产物,其单体为HOCH2CH2OH与
中含-COOC-及端基原子和原子团,为缩聚产物,其单体为HOCH2CH2OH与 ,故B正确;
,故B正确;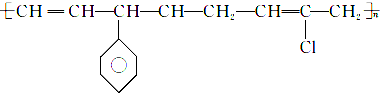 中主链只含C,为加聚反应产物,则单体为乙炔、苯乙烯、2-氯-1,3-丁二烯,故D正确;
中主链只含C,为加聚反应产物,则单体为乙炔、苯乙烯、2-氯-1,3-丁二烯,故D正确;

科目:高中化学 来源: 题型:
| 实验次数编号 | 待 待测盐酸体积(mL) | 滴入Na2CO3 溶液体积(mL) |
| 1 | 20.00 | 19.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C、向水中加入少量固体Na,平衡正向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
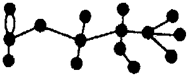 某有机物含有C、H、O三种元素,其球棍模型如图所示.该有机物可能发生的反应有①水解反应 ②加聚反应 ③取代反应 ④消去反应 ⑤银镜反应( )
某有机物含有C、H、O三种元素,其球棍模型如图所示.该有机物可能发生的反应有①水解反应 ②加聚反应 ③取代反应 ④消去反应 ⑤银镜反应( )| A、①②③④⑤ | B、①③④⑤ |
| C、①③④ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2 g Fe投入到400mL 1mol/L的硝酸中充分反应,转移电子总数为0.2NA |
| B、标准状况下,11.2LC2H6含3NA个C-H极性共价键 |
| C、标准状况下,5.6LNO和5.6LO2混合后的分子总数为0.5NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取3.23gNaCl固体 |
| B、用50 mL量筒量取30.12mL水 |
| C、向小试管中加入100mL稀盐酸 |
| D、用胶头滴管取约1mL溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com