
【题目】铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为_______________;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是_________________________。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为____________,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____Si(填“>”、“<”)。
(3)SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为_________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_________。
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______,B与N之间形成_________键。
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为________,在SiC中,每个C原子周围最近的C原子数目为___个;若晶胞的边长为a pm,则金刚砂的密度表达式为_________g/cm3。
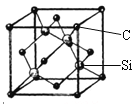
【答案】1s22s22p63s23p63d104s1或[Ar]3d104s1 CuO中铜的价层电子排布为3d94s0,Cu2O中铜的价层电子排布为3d10,后者处于稳定的全充满状态而前者不是 V形、正四面体形 > 分子晶体 sp2 sp3 配位 原子晶体 12 ![]() 或
或![]()
【解析】
(1)Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1;CuO中铜的价层电子排布为3d94s0(1分),Cu2O中铜的价层电子排布为3d10,3d10为稳定结构,所以在高温时,能生成Cu2O;
(2)硒、硅均能与氢元素形成气态氢化物分别为H2Se,SiH4,其分子结构分别V形,正四面体;若“Si-H”中键合电子偏向氢原子,说明硅显正价,氢气与硒反应时单质硒是氧化剂,硒显负价,所以硒与硅的电负性相对大小为Se>Si;
(3)SeO2常温下白色晶体,熔、沸点低,为分子晶体;二氧化硒分子中价层电子对=2+![]() (6-2×2)=3,Se原子的杂化类型为sp2,且含有一个孤电子对,所以属于V形;
(6-2×2)=3,Se原子的杂化类型为sp2,且含有一个孤电子对,所以属于V形;
(4)BF3NH3中B原子含有3个σ 键和1个配位键,所以其价层电子数是4,B原子采取sp3杂化,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,所以B、N原子之间形成配位键;
(5)金刚砂(SiC)的硬度为9.5,属于原子晶体;每个碳原子连接4个硅原子,每个硅原子又连接其它3个碳原子,所以每个碳原子周围最近的碳原子数目为3×4=12;该晶胞中C原子个数=8×![]() +6×
+6×![]() =4,Si原子个数为4,晶胞边长=a×10-10cm,体积V=(a×10-10cm)3,ρ=
=4,Si原子个数为4,晶胞边长=a×10-10cm,体积V=(a×10-10cm)3,ρ=![]() =
=![]() 或
或![]() gcm3。
gcm3。


科目:高中化学 来源: 题型:
【题目】t℃时,将0.5mol/L的氨水逐滴加入10.00mL0.5mol/L盐酸中,溶液中温度变化曲线Ⅰ、pH变化曲线Ⅱ与加入氨水的体积的关系如图所示(忽略混合时溶液体积的变化)。下列说法正确的是( )

A.Kw的比较:a点比b点大
B.b点氨水与盐酸恰好完全反应,且溶液中c(NH4+)=c(Cl-)
C.c点时溶液中c(NH4+)=c(Cl-)=c(OH-)=c(H+)
D.d点时溶液中c(NH3H2O)+2c(OH-)=c(NH4+)+2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法正确
A.该化合物仅含碳、氢两种元素B.该化合物中碳、氢原子个数比为1:3
C.无法确定该化合物是否含有氧元素D.该化合物中一定含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值。下列说法正确的是
A.25℃,1LpH=13的氢氧化钡溶液中含OH-的数目为0.2NA
B.12.0gNaHSO4晶体中阳离子和阴离子的总数为0.3NA
C.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
D.4.2gCaH2与水完全反应,转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
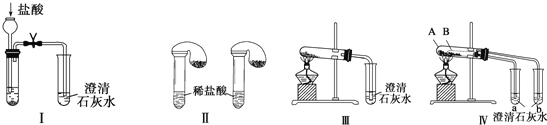
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)_____。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为____________;与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)____________。
a.Ⅳ比Ⅲ复杂 b.Ⅳ比Ⅲ安全 c.Ⅳ比Ⅲ操作简便 d.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式________。
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当石灰水过量时,其离子方程式为_________________ ;
②当碳酸氢钠与氢氧化钙物质的量之比为2∶1时,所得溶液中溶质的化学式为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯有极强的抗炎和抗氧化活性而起到抗肿瘤的作用.现设计出如下路线合成缓释药物聚咖啡酸苯乙酯:
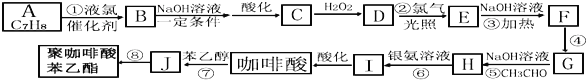
已知:B的核磁共振氢谱有三个波峰;红外光谱显示咖啡酸分子中存在碳碳双键;且:
![]() ;
;![]()
![]() 咖啡酸仅含C、H、O三种元素,蒸气密度是相同条件下
咖啡酸仅含C、H、O三种元素,蒸气密度是相同条件下![]() 的90倍,含氧质量分数为
的90倍,含氧质量分数为![]() ,则咖啡酸的分子式为 ______ ;咖啡酸可与
,则咖啡酸的分子式为 ______ ;咖啡酸可与![]() 溶液反应生成气体,1mol咖啡酸与足量钠反应生成
溶液反应生成气体,1mol咖啡酸与足量钠反应生成![]()
![]() ,咖啡酸中所有含氧官能团的名称: _____;
,咖啡酸中所有含氧官能团的名称: _____;
![]() 写出下列反应的类型:
写出下列反应的类型:![]() ______ ,
______ ,![]() ______ .
______ .
![]() 写出反应
写出反应![]() 的化学方程式: ______ .
的化学方程式: ______ .
![]() 写出反应
写出反应![]() 的化学方程式: ______ .
的化学方程式: ______ .
![]() 满足下列条件的咖啡酸的同分异构体有 ______ 种.任写三种 ______ .
满足下列条件的咖啡酸的同分异构体有 ______ 种.任写三种 ______ .
![]() 含有两个羧基
含有两个羧基![]() 苯环上有三个取代基.
苯环上有三个取代基.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语或模型正确的是
A. HF的电子式:![]() B. 用核素符号表示中子:
B. 用核素符号表示中子:![]()
C. HClO的结构式:H-Cl-O D. 用电子式表示CO2的形成过程: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源危机当前是一个全球性问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是__(填字母)。
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,不使用煤、石油等化石燃料
D.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
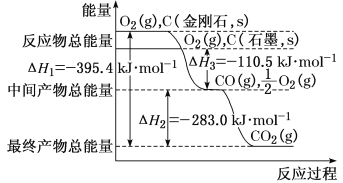
①在通常状况下,金刚石和石墨相比较,__(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=___。
②12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为__kJ。
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1。N2(g)+O2(g)=2NO(g)ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为__。
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工艺即化工技术或化学生产技术,指将原料物主要经过化学反应转变为产品的方法和过程,包括实现这一转变的全部措施。工业上用赤铁矿(含![]() 、
、![]() ,也含有
,也含有![]() 、
、![]() 、
、![]() 、
、![]() 等)制备绿矾
等)制备绿矾![]() 的工艺流程如下图:
的工艺流程如下图:
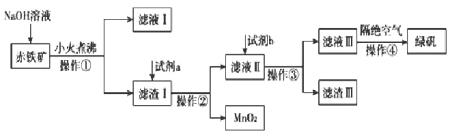
(1)操作①的名称是______________。
(2)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为_________、__________。
(3)向滤渣Ⅰ中加入过量的试剂a名称为__________,加入过量试剂b后所得滤渣Ⅲ的主要成分化学式为__________。
(4)操作③需要的玻璃仪器主要包括________________。
(5)操作④需要隔绝空气的主要原因可能是什么?___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com