
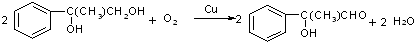
 ;
;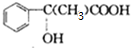 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +(n-1)H2O.
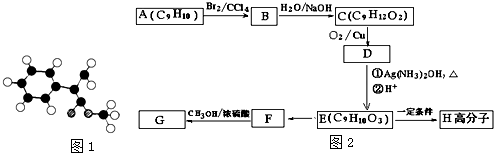
+(n-1)H2O. 分析 肉桂酸甲酯分子式为C10H10O2,G为肉桂酸甲酯的一种同分异构体,根据其分子结构模型可知G的结构为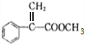 ,F与甲醇发生酯化反应生成G,故F为
,F与甲醇发生酯化反应生成G,故F为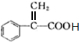 ,根据转化关系可知,A与溴发生加成得B,B发生水解得C,比较A和C的分子式结合F的结构简式可知,A为
,根据转化关系可知,A与溴发生加成得B,B发生水解得C,比较A和C的分子式结合F的结构简式可知,A为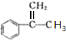 ,A与溴发生加成反应生成B,B为
,A与溴发生加成反应生成B,B为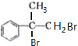 ,B在氢氧化钠水溶液发生水解反应生成C,故C为
,B在氢氧化钠水溶液发生水解反应生成C,故C为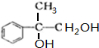 ,C催化氧化生成D,D为
,C催化氧化生成D,D为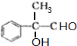 ,D被银氨溶液氧化,酸化生成E,E为
,D被银氨溶液氧化,酸化生成E,E为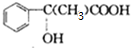 ,E发生缩聚反应生成高聚物H,H为
,E发生缩聚反应生成高聚物H,H为 ,据此解答.
,据此解答.
解答 解:肉桂酸甲酯分子式为C10H10O2,G为肉桂酸甲酯的一种同分异构体,根据其分子结构模型可知G的结构为 ,F与甲醇发生酯化反应生成G,故F为
,F与甲醇发生酯化反应生成G,故F为 ,根据转化关系可知,A与溴发生加成得B,B发生水解得C,比较A和C的分子式结合F的结构简式可知,A为
,根据转化关系可知,A与溴发生加成得B,B发生水解得C,比较A和C的分子式结合F的结构简式可知,A为 ,A与溴发生加成反应生成B,B为
,A与溴发生加成反应生成B,B为 ,B在氢氧化钠水溶液发生水解反应生成C,故C为
,B在氢氧化钠水溶液发生水解反应生成C,故C为 ,C催化氧化生成D,D为
,C催化氧化生成D,D为 ,D被银氨溶液氧化,酸化生成E,E为
,D被银氨溶液氧化,酸化生成E,E为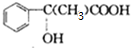 ,E发生缩聚反应生成高聚物H,H为
,E发生缩聚反应生成高聚物H,H为 ,
,
①E为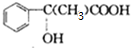 ,E中的官能团为羟基、羧基,故答案为:羟基、羧基;
,E中的官能团为羟基、羧基,故答案为:羟基、羧基;
②根据上面分析可知,E→F的反应类型是消去反应,故答案为:消去反应;
③C→D的化学方程式为 ,E→H的化学方程式为n
,E→H的化学方程式为n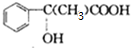 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +(n-1)H2O,
+(n-1)H2O,
故答案为: ;n
;n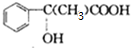 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +(n-1)H2O.
+(n-1)H2O.
点评 本题考查有机物的推断,是对有机知识的综合运用,能较好的考查考生的阅读、自学能力和思维能力,根据G的分子式,结合有关G的信息,推断G的结构是解题的关键,再结合反应条件、反应信息进行推断其它物质,难度中等,是热点题型.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子学说 | B. | 分子学说 | C. | 等电子体学说 | D. | 元素周期律 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CO2中含有原子数NA | |
| B. | 1mol/L的硫酸钠溶液中,所含Na+数为2NA | |
| C. | 标准状况下,11.2 L水所含分子数为0.5 NA | |
| D. | 1 mol Fe和足量盐酸完全反应失去的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ①④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com