
”¾ĢāÄæ”æ4.35g¶žŃõ»ÆĆĢÄÜÓė×ćĮæÅØŃĪĖį£ØĆܶČĪŖ1.19gcm©3”¢ÖŹĮæ·ÖŹżĪŖ36.5%£©ĶźČ«·“Ó¦£®Ēó£ŗ
£Ø1£©ÅØŃĪĖįÖŠHClµÄĪļÖŹµÄĮæÅØ¶Č£ŗc£ØHCl£©= £®
£Ø2£©±»Ńõ»ÆµÄHClµÄĪļÖŹµÄĮæ£ŗn£ØHCl£©= £®
”¾“š°ø”æ
£Ø1£©11.9mol/L
£Ø2£©0.1mol
”¾½āĪö”æ½ā£ŗ£Ø1£©øł¾Żc= ![]() æÉÖŖ£¬ĆܶČĪŖ1.19gcm©3”¢ÖŹĮæ·ÖŹżĪŖ36.5%ÅØŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ
æÉÖŖ£¬ĆܶČĪŖ1.19gcm©3”¢ÖŹĮæ·ÖŹżĪŖ36.5%ÅØŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ ![]() mol/L=11.9mol/L£¬
mol/L=11.9mol/L£¬
ĖłŅŌ“š°øŹĒ£ŗ11.9mol/L£»
£Ø2£©4.35g¶žŃõ»ÆĆĢµÄĪļÖŹµÄĮæĪŖ ![]() =0.05mol£¬Ōņ£ŗ
=0.05mol£¬Ōņ£ŗ
MnO2+4HCl£ØÅØ£© | Cl2”ü+2H2O |
1 | 1 |
0.05mol | n£ØCl2£© |
¹Źn£ØCl2£©=0.05mol
±»Ńõ»ÆµÄHClÉś³ÉCl2£¬øł¾ŻĀČŌ×ÓŹŲŗćæÉÖŖ£¬±»Ńõ»ÆµÄHClµÄĪļÖŹµÄĮæŹĒCl2µÄ2±¶£¬¹Ź±»Ńõ»ÆµÄHClĪŖ0.05mol”Į2=0.1mol£¬
ĖłŅŌ“š°øŹĒ£ŗ0.1mol£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹµÄ±ä»Æ¹ż³ĢÖŠ£¬ÓŠ¹²¼Ū¼üĆ÷ĻŌ±»ĘĘ»µµÄŹĒ£Ø £©
¢ŁI2Éż»Ŗ
¢ŚNaClæÅĮ£±»·ŪĖé
¢ŪHClČÜÓŚĖ®µĆŃĪĖį
¢Ü“ÓNH4HCO3ÖŠĪŵ½ĮĖ“Ģ¼¤ŠŌĘųĪ¶£®
A.¢Ł¢Ś
B.¢Ś¢Ū
C.¢Ł¢Ü
D.¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø14·Ö£© Éé£ØAs£©ŹĒµŚĖÄÖÜĘŚ¢õA×åŌŖĖŲ£¬æÉŅŌŠĪ³ÉAs2O3”¢As2O5”¢H3AsO3”¢H3AsO4µČ»ÆŗĻĪļ£¬ÓŠ×Źć·ŗµÄÓĆĶ¾”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©»³öÉéµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼”£
£Ø2£©¹¤ŅµÉĻ³£½«ŗ¬Éé·ĻŌü£ØÖ÷ŅŖ³É·ÖĪŖAs2O3£©ÖĘ³É½¬×“£¬ĶØČėO2Ńõ»Æ£¬Éś³ÉH3AsO4ŗĶµ„ÖŹĮņ”£Š“³ö·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½”£øĆ·“Ó¦ŠčŅŖŌŚ¼ÓŃ¹ĻĀ½ųŠŠ£¬ŌŅņŹĒ”£
£Ø3£©ŅŃÖŖ£ŗAs(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) ¦¤H1H2(g)+
H2(g)+2O2(g)=H3AsO4(s) ¦¤H1H2(g)+ ![]() O2(g)=H2O(l) ¦¤H2
O2(g)=H2O(l) ¦¤H2
2As(s)+ ![]() O2(g) =As2O5(s) ¦¤H3
O2(g) =As2O5(s) ¦¤H3
Ōņ·“Ó¦As2O5(s) +3H2O(l)= 2H3AsO4(s)µÄ¦¤H =”£
£Ø4£©298 KŹ±£¬½«20 mL 3x mol”¤L1 Na3AsO3”¢20 mL 3x mol”¤L1 I2ŗĶ20 mL NaOHČÜŅŗ»ģŗĻ£¬·¢Éś·“Ó¦£ŗAsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)”£ČÜŅŗÖŠc(AsO43)Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
AsO43(aq)+2I(aq)+ H2O(l)”£ČÜŅŗÖŠc(AsO43)Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ 
¢ŁĻĀĮŠæÉÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ£ØĢī±źŗÅ£©”£
a.ČÜŅŗµÄpH²»ŌŁ±ä»Æ
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)²»ŌŁ±ä»Æ
d. c(I)=y mol”¤L1
¢ŚtmŹ±£¬vÕż vÄę£ØĢī”°“óÓŚ”±”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£
¢ŪtmŹ±vÄę tnŹ±vÄę£ØĢī”°“óÓŚ”±”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©£¬ĄķÓÉŹĒ”£
¢ÜČōĘ½ŗāŹ±ČÜŅŗµÄpH=14£¬ŌņøĆ·“Ó¦µÄĘ½ŗā³£ŹżKĪŖ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æClO2ŹĒŅ»ÖÖĻū¶¾É±¾śŠ§ĀŹøß”¢¶ž“ĪĪŪČ¾Š”µÄĖ®“¦Ąķ¼Į£®ŹµŃéŹŅæÉĶعżŅŌĻĀ·“Ó¦ÖʵĆClO2£ŗ2KClO3+H2C2O4+H2SO4 ![]() 2ClO2”ü+K2SO4+2CO2”ü+2H2O£®
2ClO2”ü+K2SO4+2CO2”ü+2H2O£®
ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø £©
A.KClO3ŌŚ·“Ó¦ÖŠµĆµ½µē×Ó
B.ClO2ÖŠĀȵĻÆŗĻ¼ŪĪŖ+4¼Ū
C.ŌŚ·“Ó¦ÖŠH2C2O4ŹĒ»¹Ō¼Į
D.1 mol KClO3²Ī¼Ó·“Ó¦ÓŠ2molµē×Ó×ŖŅĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒŹµŃéŹŅÖʱøĀČĘų²¢½ųŠŠŅ»ĻµĮŠĻą¹ŲŹµŃéµÄ×°ÖĆ£Ø¼Š³Ö¼°¼ÓČČŅĒĘ÷ŅŃĀŌ£©£®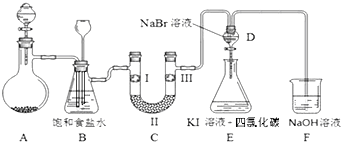
£Ø1£©ÖʱøĀČĘųŃ”ÓƵÄŅ©Ę·ĪŖ¶žŃõ»ÆĆĢŗĶÅØŃĪĖį£¬ŌņĻą¹ŲµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ £®
£Ø2£©×°ÖĆBÖŠ±„ŗĶŹ³ŃĪĖ®µÄ×÷ÓĆŹĒ £®
£Ø3£©×°ÖĆCµÄŹµŃéÄæµÄŹĒŃéÖ¤ĀČĘųŹĒ·ń¾ßÓŠĘư׊Ō£¬ĪŖ“ĖCÖŠ¢ń”¢¢ņ”¢¢óŅĄ“Ī·ÅČė £®
a | b | c | d | |
¢ń | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ |
¢ņ | ¼īŹÆ»Ņ | ĪŽĖ®CaCl2 | ÅØĮņĖį | ĪŽĖ®CaCl2 |
¢ó | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ |
£Ø4£©Éč¼Ę×°ÖĆD,EµÄÄæµÄŹĒ±Č½ĻĀČ”¢ä唢µāµ„ÖŹµÄŃõ»ÆŠŌĒæČõ£®µ±ĻņDÖŠ»ŗ»ŗĶØČėŅ»¶ØĮæĀČĘųŹ±£¬æÉŅŌ擵½ĪŽÉ«ČÜŅŗÖš½„±äĪŖÉ«£¬“ņæŖD×°ÖĆÖŠ»īČū£¬½«DÖŠÉŁĮæČÜŅŗ¼ÓČė×°ÖĆEÖŠ£¬Õńµ“£®¹Ū²ģµ½µÄĻÖĻóŹĒ £® ¾ČĻÕęæ¼ĀĒ£¬ÓŠĶ¬Ń§Ģį³öøĆŹµŃé·½°øČŌÓŠ²»×ć£¬ĒėĖµĆ÷ĘäÖŠ²»×ćµÄŌŅņŹĒ £®
£Ø5£©×°ÖĆFÖŠÓĆ×ćĮæNaOHČÜŅŗĪüŹÕŹ£ÓąµÄĀČĘų£¬ŹŌŠ“³öĻąÓ¦µÄ»Æѧ·½³ĢŹ½£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫pHĪŖ5µÄĮņĖįČÜŅŗĻ”ŹĶ500±¶£¬Ļ”ŹĶŗóČÜŅŗÖŠc£Ø ![]() £©£ŗc£ØH+£©Ō¼ĪŖ£Ø £©
£©£ŗc£ØH+£©Ō¼ĪŖ£Ø £©
A.1£ŗ1
B.1£ŗ2
C.1£ŗ10
D.10£ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŚnµē×Ó²ćµ±Ėü×÷ĪŖ×īĶāµē×Ó²ćŹ±£¬×ī¶ąČŻÄɵĵē×ÓŹżÓėn-1²ćĻąĶ¬£¬µ±Ėü×÷ĪŖŌ×ӵēĪĶā²ćŹ±£¬Ęäµē×ÓŹż±Čn+1²ć×ī¶ąČŻÄɵĵē×ÓŹż¶ą10øö£¬Ōņ“Ėµē×Ó²ćŹĒ£Ø £©
A.KB.LC.MD.N
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢WĖÄÖÖĪļÖŹÓŠČēĶ¼ĖłŹ¾Ļą»„×Ŗ»Æ¹ŲĻµ£®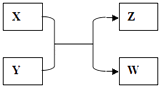
£Ø1£©ČōZ”¢WŹĒĮ½ÖÖĖį£¬X»ĘĀĢÉ«ĘųĢ壬Ōņ£ŗX”¢Y·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£»Z”¢WµÄ»ģŗĻČÜŅŗ¾ĆÖĆŗóµÄ³É·ÖŹĒ£ØĢī»ÆѧŹ½£©£®
£Ø2£©ČōX”¢WŹĒĮ½ÖÖ½šŹō£¬WµÄŗĻ½šÓĆÓŚÖĘŌģČĖŌģ¹Ē÷Ą£¬ÓėČĖĢåÓŠŗÜŗƵÄČŚŗĻŠŌ£¬øĆ·“Ó¦³£ÓĆÓŚŅ±Į¶¹óÖŲ½šŹō£®Ōņ£ŗXŌŚæÕĘųÖŠ±ä°µµÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø3£©ČōX”¢YŹĒµ„ÖŹ£¬Z”¢W¾łĪŖ»ÆŗĻĪļ£¬WµÄĦ¶ūÖŹĮæ±ČZøß71£¬Ōņ£ŗZµÄ»ÆѧŹ½ĪŖ £® ÓŠ°×ŃĢÉś³ÉµÄ»Æѧ·½³ĢŹ½ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×éŌŚŹµŃéŹŅÉč¼ĘĮĖĻĀĮŠŹµŃé×°ÖĆÖĘČ”ĘÆ°×·Ū£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹéŠ“ŹµŃéŹŅÖʱøĀČĘų»Æѧ·½³Ģ £®
£Ø2£©Ķ¼¼×ÖŠµĪ¼ÓÅØŃĪĖįµÄ×°ÖĆĆū³Ę £¬ ŅŅ×°ÖƵÄ×÷ÓĆŹĒ £®
£Ø3£©ČōÓĆŗ¬ÓŠ0.4mol HClµÄÅØŃĪĖįÓė×ćĮæµÄMnO2·“Ó¦ÖĘĀČĘų£¬ÖʵƵÄĀČĘųĢå»ż£Ø±ź×¼×“æöĻĀ£©×ÜŹĒŠ”ÓŚ2.24L µÄŌŅņŹĒ £®
£Ø4£©ĘÆ°×·ŪµÄÓŠŠ§³É·ÖµÄĆū³ĘŹĒ £¬ ĘÆ°×·ŪŌŚæÕĘųÖŠ³¤ĘŚ·ÅÖĆŹ§Š§µÄ»Æѧ·½³Ģ”¢ £®
£Ø5£©øĆŠĖȤŠ”×éÓĆ100mL 12mol/LŃĪĖįÓė8.7g MnO2ÖʱøĀČĘų£¬²¢½«ĖłµĆĀČĘųÓė¹żĮæµÄŹÆ»ŅČé·“Ó¦£¬ŌņĄķĀŪÉĻ×ī¶ąæÉÖʵĆgĘÆ°×·Ū£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com