
| A. | NO2、Cl2O7都是酸性氧化物 | B. | 水银、水玻璃都是混合物 | ||
| C. | 干冰、可燃冰都是分子晶体 | D. | HD、HCHO都是极性分子 |
分析 A.酸性氧化物是和碱反应生成盐和水的氧化物,反应为复分解反应,生成一种盐和水;
B.不同物质组成的为混合物;
C.干冰是二氧化碳固体,可燃冰是甲烷固体,都是分子构成;
D.HD是氢气单质属于非极性分子;
解答 解:A.和碱反应生成盐和水的氧化物为酸性氧化物,NO2和碱反应发生的是氧化还原反应,不是酸性氧化物,Cl2O7是高氯酸的酸酐,和碱反应生成盐和水属于酸性氧化物,故A错误;
B.水银为金属汞,属于纯净物,水玻璃是硅酸钠的水溶液,属于混合物,故B错误;
C.干冰是二氧化碳固体,可燃冰是甲烷晶体,都是分子晶体,故C正确;
D.HD为氢气分子,是非极性分子,HCHO是极性分子,故D错误;
故选C.
点评 本题考查了物质分类方法、物质组成、物质结构和性质的理解应用,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6 LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 78 g苯含有C=C双键的数目为3 NA | |
| C. | 1 L1mol•L-1的CuSO4溶液中含NA个Cu2+ | |
| D. | 常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2 具有氧化性,可用于漂白纸浆 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 明矾能水解生成Al(OH)3 胶体,可用作净水剂 | |
| D. | FeCl3 溶液能与Cu 反应,可用于蚀刻印刷电路 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
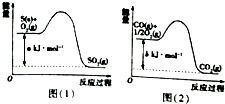
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b-a)kJ•mol-1 | |
| B. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(b-a)kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2b-a)kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b+a)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 25.02 |
| 2 | 20.00 | 0.20 | 28.80 |
| 3 | 20.00 | 1.30 | 26.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①② | C. | ①③ | D. | ①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com