
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,在空气中能产生丁达尔现象 |
| B、在海轮外壳上镶嵌锌块,会减缓船体的锈蚀 |
| C、经过必要的化学变化能从海水中提取NaCl、Mg、Br2等物质 |
| D、大量燃烧化石燃料排放的废气中大量CO2、SO2,造成大气污染,从而使雨水的PH=5.6形成酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
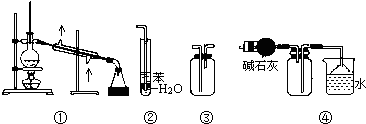
| A、装置①常用于分离互相溶解且沸点相差10℃以上的液态混合物 |
| B、装置②可用于吸收NH3或HCl气体,并防止到吸 |
| C、装置③可用于收集H2、CO2、Cl2、NH3等气体 |
| D、装置④可用于干燥、收集氨气,若将碱石灰改成五氧化二磷,可用于干燥、收集氯化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| n(H2) |
| n(CO2) |
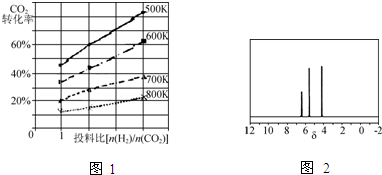
查看答案和解析>>
科目:高中化学 来源: 题型:
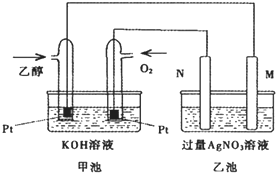 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将11.2L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
| B、100mL 1mol?L-1 Na[Al(OH)4]溶液中含有0.1NA个[Al(OH)4]- |
| C、标准状况下,22.4L NO和22.4L O2混合后所得气体中分子总数为NA |
| D、标准状况下,1.12L 1H2和0.2g 2H2均含有0.1NA个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在c(HCO3-)=0.1mol/L的溶液中:NH4+、Al3+、Cl-、NO3- |
| B、在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe2+、ClO-、Na+、SO42- |
| C、在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+ |
| D、pH=1的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚钠溶液中通入CO2气体后产生白色沉淀,通过抽滤可分离出苯酚 |
| B、滴定实验时,锥形瓶用蒸馏水洗净后,直接盛待测液 |
| C、基于硫代硫酸钠与稀硫酸反应生成S和SO2,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测SO2体积,计算出其的反应速率 |
| D、某溶液加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液含有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com