
| A. | 硝基苯的结构简式: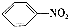 | B. | 氯化铵的电子式: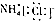 | ||
| C. | 甲烷的球棍模型: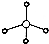 | D. | 乙醇的结构简式:CH3CH2OH |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 石油分馏后得到的汽油、柴油、煤油等都是纯净物 | |
| B. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”才能提高空气质量 | |
| C. | 太阳能电池板中的硅元素在元素周期表中处于金属与非金属的交界位置 | |
| D. | 煤经过气化和液化两个物理变化,可变为清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | Ba(OH)2与H2SO4反应:H++OH-=H2O | |
| C. | 铁与醋酸反应:Fe+2H+=Fe2++H2↑ | |
| D. | NaHCO3与NaOH反应:HCO3-+OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 禁止用工业酒精配制饮用酒和调味用的料酒 | |
| D. | 溴乙烷、TNT、葡萄糖都是无色溶于水的有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
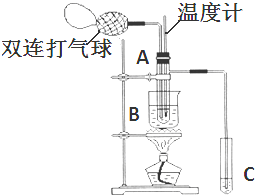
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑤ | C. | 只有⑤ | D. | 只有② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅是制造太阳能电池的常用材料 | |
| B. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 | |
| C. | Na2O2可用作呼吸面具中的供氧剂 | |
| D. | 二氧化硅是制造光导纤维的材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com