
| A. | 空气、硫酸铜、硫酸 | B. | 乙酸、空气、纯碱 | ||
| C. | 氧化铁、胆矾、熟石灰 | D. | 硝酸、蔗糖水、氢氧化铁 |
科目:高中化学 来源: 题型:选择题
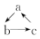 (“→”表示反应一步完成)关系转化的是( )
(“→”表示反应一步完成)关系转化的是( )| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | NaOH | NaHCO3 | Na2CO3 |
| C | Al | Al(OH)3 | Al2O3 |
| D | MgCl2 | Mg(OH)2 | MgO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g NH3所含的电子数是 10NA | |
| B. | 常温常压下,22.4L氧气含氧原子数为2NA | |
| C. | 0.5 mol/L K2SO4溶液中含有NA个K+离子 | |
| D. | 2.3g金属钠与氧气反应全部生成Na2O时失去的电子数是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaHCO3溶液中滴加澄清石灰水,不会产生沉淀 | |
| B. | 等质量NaHCO3和Na2CO3分别与足量盐酸反应,生成的CO2在同温同压下体积相同 | |
| C. | 向Na2CO3溶液中缓慢通入等物质的量的HCl,生成的CO2与原Na2CO3的物质的量之比为1:2 | |
| D. | 向Na2CO3饱和溶液中通入CO2,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在容量瓶中定容时,俯视刻度线 | |
| B. | 用量筒量取浓盐酸时,俯视刻度线 | |
| C. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验溶液中是否含有Fe2+时,所用KMnO4溶液用硫酸酸化 | |
| B. | 检验溶液中是否含有Br-时,所用AgNO3溶液用盐酸酸化 | |
| C. | 检验溶液中是否含有SO32-时,所用BaCl2溶液用硝酸酸化 | |
| D. | 检验溶液中是否含有SO42-时,所用BaCl2溶液用硝酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量就是1摩尔物质的质量 | B. | 1 mol水中含有2 mol氢和1 mol氧 | ||
| C. | 1 molH2中含有6.02个氢分子 | D. | NH3的摩尔质量是17g•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com