
����Ŀ����ѧʵ�����������⻯ѧ֪ʶ���γɻ�ѧ������̽���봴��������
��1���������Ͽ�֪��2KMnO4+16HCl��Ũ���T 2MnCl2 + 2KCl + 5Cl2�� + 2H2O��ijͬѧ���ͼ1��ʾװ�����Ʊ����������������������ʵ��װ�û��Լ��д������______
A �٢� B �� C �ڢ� D �٢�


��2����ͼ1װ������ȷ���������ռ�Cl2��װ�ã����ͼ2��ѡ�ú��ʵ�װ��__��
��3�����Ƶõ�Cl2��������ʵ�飬װ����ͼ3��ʾ������װ��ʡ�ԣ�����ش��������⡣
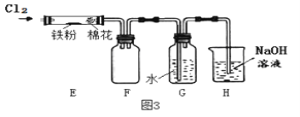
��װ��E�пɹ۲쵽____����Ӧ�Ļ�ѧ����ʽ____��
��װ��F�ڷ�Ӧ�е�������_____��
��װ��G���õ���Һ�о���Ư���Եķ�����___��
��װ��H������____��
��4����ҵƯ�۳���Cl2��ʯ���鷴Ӧ�Ƶã���Ӧ����ʽΪ______��
���𰸡�C C ���ҷ�Ӧ�������غ�(��)ɫ���� 2Fe+3Cl2![]() 2FeCl3 ������ HClO β������(������������) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2FeCl3 ������ HClO �����(������������) 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
��������
(1)KMnO4��ŨHCl�ڳ����·�Ӧ����Cl2��Ũ�����ӷ����ӷ���װ�����ɵ������к��лӷ���HCl��ˮ�������ʣ�Ӧͨ��ʢ�б���ʳ��ˮ��ϴ��ƿ��ȥHCl��Ȼ��ͨ��ʢ��Ũ�����ϴ��ƿ���и���ݴ˽��
(2)�����ж����ܶȱȿ����ݴ˽��
(3)���������ڼ��ȵ������¾��ҷ�Ӧ�������غ�ɫ���̣�����Ϊ�Ȼ�����װ��F�����ܶ�Ϊ�̵ģ��ڷ�Ӧ�е������Ƿ�ֹ������װ��G���õ���ҺΪ������ˮ�����о���Ư���Եķ�����HClO�������ж���װ��Hװ������������Һ����������Ӧ����β�����������á�
��4����ҵƯ�۳���Cl2��ʯ���鷴Ӧ�Ƶã�ʯ����ijɷ���Ca(OH)2��
(1)KMnO4��ŨHCl�ڳ����·�Ӧ����Cl2���ʢ���ȷ��Ũ�����ӷ����ӷ���װ�����ɵ������к��лӷ���HCl��ˮ�������ʣ�����ѡ������������Һ����Ϊ����Ҳ�ܺ�NaOH��Ӧ��Ӧ��ʹ�ñ���ʳ��ˮ�ʢڴ������������������Ũ������������Ӧ�ó�����ֱ��ͨ��Ũ�����У���������Ӧ�����̳����ʢ۴��ʴ�ΪC��
(2)�������ܶȴ��ڿ������ж�������ѡ�������ſ������ռ���Ӧ����β������������ֱ���ŷŵ������У���Ӧ��ѡ��װ��C��
(3)��װ��E�����������ڸ��������¾��ҷ�Ӧ�������غ�(��)ɫ���̣���Ӧ�Ļ�ѧ����ʽΪ��2Fe+3Cl2![]() 2FeCl3��
2FeCl3��
��װ��F�����ܶ�Ϊ�̵ģ��ڷ�Ӧ�е������Ƿ�ֹ������
��װ��G���õ���ҺΪ������ˮ�����о���Ư���Եķ�����HClO��
�������ж�������������ֱ���ŷŻ���ɿ�����Ⱦ��װ��Hװ������������Һ����������Ӧ����β�����������á�
��4����ҵƯ�۳���Cl2��ʯ���鷴Ӧ�Ƶã���ѧ����ʽΪ��2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O��


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�ѧ�������������ת����˵��������ǣ� ��
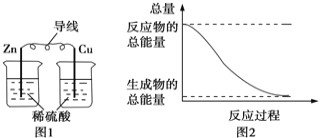
A.ͼ1��ʾ��װ���ܽ���ѧ��ת��Ϊ����
B.ͼ2��ʾ�ķ�ӦΪ���ȷ�Ӧ
C.�кͷ�Ӧ�У���������������ȷ�Ӧ�����������
D.��ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ������γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ž��з���Ԫ��������150���ꡣ�±���Ԫ�����ڱ���һ���֣�W��X��Y��ZΪ����������Ԫ�أ�W��X������ϼ�֮��Ϊ8������˵���������
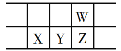
A. ԭ�Ӱ뾶��W<X
B. ���³�ѹ�£�Y����Ϊ��̬
C. ��̬�⻯�����ȶ��ԣ�Z<W
D. X������������ˮ������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��Һ���ǿ�ѧ�ҽ������Ƴ���һ��ʹɳĮ�������¼�������������ɳĮ������һ�����ľ۱�ϩ����(![]() )��ˮ��Һ������ˮ��Һ���еĸ߷��ӻ�������ɳ�����ӽ�ϣ��ڵر���30��50cm���γ�һ����0.5cm�ĸ�ˮ�㣬������ֹ���µ��η��������������������ˮ�����á����жԾ۱�ϩ������˵���У�����ȷ���ǣ� ��
)��ˮ��Һ������ˮ��Һ���еĸ߷��ӻ�������ɳ�����ӽ�ϣ��ڵر���30��50cm���γ�һ����0.5cm�ĸ�ˮ�㣬������ֹ���µ��η��������������������ˮ�����á����жԾ۱�ϩ������˵���У�����ȷ���ǣ� ��
A.��һ���������ܷ����ӳɷ�Ӧ
B.������CH2=CH��COOR�����ӳɾۺϷ�Ӧ���õ�
C.��һ���������ܷ���ˮ�ⷴӦ
D.�ϳ�����С���ӻ�������CH2=CH��COOR
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000mol��L-1 ������ζ� 20.00 mL δ֪Ũ�ȵİ�ˮ���ζ�������ͼ��ʾ���μ� 20. 00 mL ����ʱ������Һ�� c (Cl-)= c( NH4+)+c(NH3��H2O)+c( NH3)������˵���������

A.�����Һ�� c( NH4+)+c ( NH3��H2O)+c(NH3)=2c (Cl-)
B.�����Һ�� c( NH4+)=c (Cl-)
C.�����Һ�� c (Cl-)> c( H+)>c (NH4+)>c(OH-)
D.�ð�ˮ��Ũ��Ϊ 0.1000mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ�����Ժ�������(��Ҫ�ɷ�ΪNiO������������ FeO��Fe2O3��CoO��BaO ��SiO2)Ϊԭ���Ʊ�NixOy ��̼����(CoCO3)�Ĺ���������ͼ��
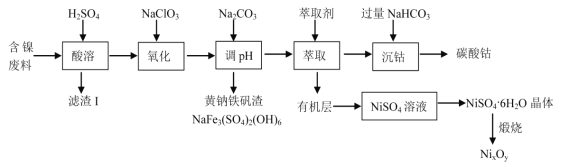
��֪�й��������↑ʼ�����ͳ�����ȫ�� pH �����
�������� | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Ni(OH)2 |
��ʼ������ pH | 1.5 | 6.5 | 7.2 | 7.7 |
������ȫ�� pH | 3.7 | 9.7 | 9.4 | 9.2 |
��ش��������⣺
(1)������������Ҫ�ɷ�Ϊ(�ѧʽ)_____��
(2)��������ʱ(���� NaClO3)�����ӷ���ʽΪ_____��
(3)���� Na2CO3 ������ pH����Ŀ�������ɻ���������������ȥ����Ҳ��ͨ������MO(��Ӧ�Ľ���������)������ pH ������ȥ���� pH ���Ƶķ�ΧΪ_____��
(4)��ʵ������ȡ����Ӧ����_____�����(����������)����ˮ���м���NaHCO3 ʱ�����ӷ���ʽΪ_________��
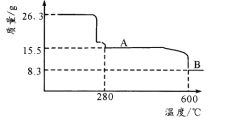
(5)�� NiSO4 ��Һ���NiSO4��6H2O ����IJ��������ǣ�_____��_________�����ˣ�ϴ�ӣ������������ʱʣ������������¶ȱ仯������ͼ���������� B ������ʾ�����������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NA�ǰ����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.1molOD-�к��е�����������������Ϊ9NA
B.60g��������12g������Ļ�����й��ۼ���Ϊ17NA
C.11.2L����������þ�۳�ַ�Ӧ��ת�Ƶĵ�����ΪNA
D.1L0.1mo1��L-1CH3COONa��Һ�У�CH3COO-��ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭת¯�̻ң���Ҫ�ɷ�ZnO����Pb��Cu��Cd��As��Cl��F��Ԫ�أ��л���п��ͭ��Ǧ��Ԫ�ؽ�����Դ�ۺ����ã�������Ҫ���塣��ͭת¯�̻��Ʊ���Ҫ����ԭ�ϻ�������п�Ĺ���������ͼ��ʾ��
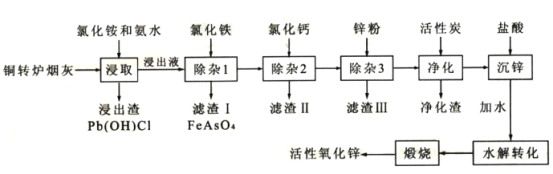
��֪������̿������Ҫ�dz�ȥ�л����ʡ�
��ش��������⣺
��1��������Һ��пԪ����[Zn(NH3)4]2+��ʽ���ڣ����ȡʱZnO������Ӧ�����ӷ���ʽΪ___��
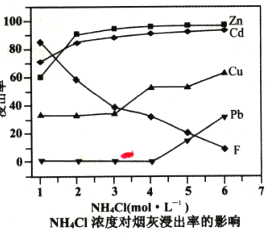
��2���ڷ�Ӧ�¶�Ϊ50�棬��Ӧʱ��Ϊlhʱ���ⶨ��Ԫ�صĽ��������Ȼ����ҺŨ�ȵĹ�ϵ��ͼ���������ͼ�������Ȼ�����˵�Ũ��Ϊ___ mo1��L-1��
��3��������Һ��c��AsO43-��=6.0��10-3molL-1���ֽ�8.0��10-3mo1L-1FeC13��Һ�����Һ�����������������������������¶�ʱKsp(FeAsO4)=2.0��10-22����Ӧ����Һ��c(AsO43-)=___mo1L-1��
��4������II����Ҫ�ɷ�Ϊ___������3���û����ӹ��̣���˹�����Ҫ��ȥ�Ľ�����___���ѧʽ����
��5����п�õ�������ΪZn(NH3)2C12����д��ˮ��ת���Ļ�ѧ����ʽ___��
��6���������п���ѭ��ʹ�õ����ʵĵ���ʽΪ___��
��7��ȡmg��������п��Ʒ��Ԥ��������ɴ���Һ������ָʾ��3��4�Σ��ټ����������Ǽ��İ�����amolL-1EDTA��Һ���еζ������ı�ҺVmL����֪����1.0mLEDTA��Һ[c(EDTA)=1.000mo1L-1]�൱���Կ˱�ʾ������п����Ϊ0.08139������Ʒ������п����������Ϊ___���ô���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1 mol/L��NaOH��Һ��ε���20 mL0.1 mol/L��CH3COOH��Һ�У�������ҺpH�仯��ͼ��ʾ�������й�˵����ȷ���ǣ� ��
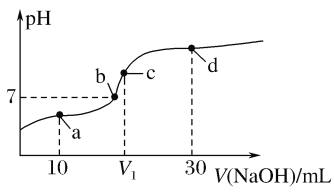
A.a�㣺c(CH3COOH)>c(CH3COO-)
B.b��Ϊ�ζ��յ�
C.��V1=20����c�㴦ˮ�ĵ���̶����
D.d�㣺c(CH3COO-)+2c(CH3COOH)=2c(OH-)-2c(H+)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com