
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案科目:高中化学 来源: 题型:
【题目】如图所示,某刚性容器内有一活塞和弹簧,B为真空,A内已充入2molSO2和lmolO2,在一定条件下发生可逆反应2SO2+O2![]() 2SO3;△H=-QkJ/mol,(Q>0)—段时间后活塞己保持静止,SO2的反应速率为Y0。再往A内迅速充入2 molSO2和lmolO2,当活塞再次保持静止时,SO2的反应速率为Y,在此过程中,下列说法正确的是
2SO3;△H=-QkJ/mol,(Q>0)—段时间后活塞己保持静止,SO2的反应速率为Y0。再往A内迅速充入2 molSO2和lmolO2,当活塞再次保持静止时,SO2的反应速率为Y,在此过程中,下列说法正确的是
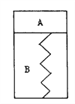
A. 活塞先下移,后上移到原静止位置,Y>Y0
B. 活塞先下移,后上移到原静止位置,Y = Y0
C. 活塞先下移,后上移但不到原静止位置,Y>Y0
D. 活塞先下移,后上移但不到原静止位置,Y = Y0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
甲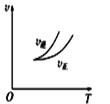 乙
乙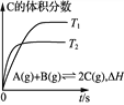 丙
丙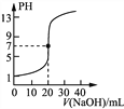 丁
丁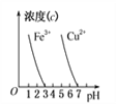
A. 由甲图甲可知正反应为放热反应
B. 乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0
C. 丙表示0.1000mol·L-1NaOH溶液滴定20.00mL0.1000mol·L-1醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入NaOH调节pH至3~4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是________,操作②的名称是____________。
(2)试剂a是____________(填化学式,下同),试剂b是__________,固体B是____________。
(3)加入试剂a所发生反应的化学方程式为__________________________________。
加入试剂b所发生反应的化学方程式为____________________________________。
(4)该方案能否达到实验目的:__________________________(填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)__________。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:a.NaOH+HCl=NaCl+H2O b.Cu+2Ag+ =Cu2+ +2Ag
(1)反应____(填字母)不能设计成原电池。原因是__________________________。
(2)a反应为______反应(填“放热”或“吸热”),NaOH和HCl的总能量________(填“大于”“小于”或“等于”)NaCl和H2O的总能量。
(3)已知HCl中H-Cl键的键能为431 kJ·mol-1,则断开1molH-Cl键_____431 kJ的能量,形成1molH-Cl键_____431 kJ的能量。(填“吸收”或“放出”)
(4)反应____(填字母)能设计成原电池,请画出实验装置图,注明电极材料和电解质溶液。__________

写出电极反应式及反应类型
正极反应式:_____________________,
反应类型:_______________________,
负极反应式:_____________________。
(5)上题所设计原电池中,向正极移动的离子为_______,电池工作一段时间后,电解质溶液质量减轻7.6g,正极增重的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
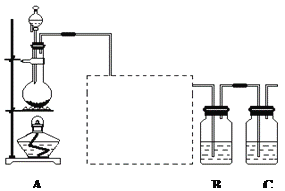
(1)装置A的分液漏斗中盛装的试剂是___________,烧瓶中加入的试剂是___________。
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用________________。
(3)装置B中盛放的试剂是______________(选填下列所给试剂的字母),实验现象为___________________,化学反应方程式是__________________________________。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因。______________________________________________________________________。
(5)已知:①硫酸比次氯酸稳定;②高氯酸比硫酸酸性强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气加热生成三氯化铁,铁与硫加热生成硫化亚铁。可说明氯比硫非金属性强的是_______。
A.全部 B.②③④⑥ C.①②④⑤⑥ D.除①以外
(6)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属性?简述你的理由____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入CO和CO2的混合气体,其密度是相同条件下氦气密度的8倍,这时测得容器内压强为P1,若控制容器的体积不变,加入足量的过氧化钠,并不断用电火花点燃至完全反应,恢复到开始的温度,再次测得容器内的压强为P2,则P1和P2关系是
A. P1=8P2 B. P1=4P2 C. P1=2P2 D. P1=P2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.lmol/L的HA溶液中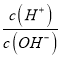 =1010,0.01mol/L的BOH溶液pH=12。请回答下列问题:
=1010,0.01mol/L的BOH溶液pH=12。请回答下列问题:
(1)HA是_________(填“强电解质”或“弱电解质”,下同),BOH是_______ 。
(2)HA的电离方程式是________。其中由水电离出的c(H+)=____mol/L。
(3)在加水稀释HA的过程中,随着水量的增加而减小的是____ (填字母)。
A. 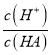 B.
B.  C. c(H+)与c(OH-)的乘积 D.c(OH-)
C. c(H+)与c(OH-)的乘积 D.c(OH-)
(4)将等体积等物质的量浓度的HA溶液和BOH溶液混合后的溶液呈________性,请用离子方程式解释其原因______________________。
(5)常温下pH=12的BOH溶液100mL,加0.01mol/LNaHSO4,使溶液的pH为11。(混合溶液体积变化忽略不计),应加NaHSO4________mL。 (保留到小数点后一位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com