
ΓΨΧβΡΩΓΩΡ≥ΧΰA0.2mol‘Ύ―θΤχ÷–Άξ»Ϊ»Φ…’ΚσΘ§…ζ≥…![]() ΓΔ
ΓΔ![]() Ης1.2molΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Ης1.2molΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΧΰAΒΡΖ÷Ή” ΫΈΣ______ΓΘ
(2)»τΧΰA≤ΜΡή ΙδεΥ°Ά …ΪΘ§ΒΪ‘Ύ“ΜΕ®ΧθΦΰœ¬Ρή¬»ΤχΖΔ…ζ»Γ¥ζΖ¥”ΠΘ§ΤδΓΣ¬»»Γ¥ζΈο÷Μ”–“Μ÷÷Θ§‘ρΧΰAΒΡΫαΙΙΦρ ΫΈΣ______ΓΘ
(3)»τ»Γ“ΜΕ®ΝΩΒΡΗΟΧΰAΆξ»Ϊ»Φ…’ΚσΘ§…ζ≥…![]() ΚΆ
ΚΆ![]() Ης3molΘ§‘ρ”–______gΧΰA≤ΈΦ”ΝΥΖ¥”ΠΘ§»Φ…’ ±œϊΚΡ±ξΉΦΉ¥Ωωœ¬ΒΡ―θΤχ______LΓΘ
Ης3molΘ§‘ρ”–______gΧΰA≤ΈΦ”ΝΥΖ¥”ΠΘ§»Φ…’ ±œϊΚΡ±ξΉΦΉ¥Ωωœ¬ΒΡ―θΤχ______LΓΘ
(4)»τΧΰAΡή ΙδεΥ°Ά …ΪΘ§‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬Θ§”κ![]() Φ”≥…Θ§ΤδΦ”≥…≤ζΈοΨ≠≤βΕ®Ζ÷Ή”÷–Κ§”–4ΗωΦΉΜυΘ§‘ρΧΰAΩ…ΡήΒΡΜζΙΙΦρ Ϋ”–(≤ΜΩΦ¬«ΝΔΧε“λΙΙ)______ΓΘ
Φ”≥…Θ§ΤδΦ”≥…≤ζΈοΨ≠≤βΕ®Ζ÷Ή”÷–Κ§”–4ΗωΦΉΜυΘ§‘ρΧΰAΩ…ΡήΒΡΜζΙΙΦρ Ϋ”–(≤ΜΩΦ¬«ΝΔΧε“λΙΙ)______ΓΘ
ΓΨ¥πΑΗΓΩ![]()
![]() 42 100.8
42 100.8 ![]()
![]()
![]()
ΓΨΫβΈωΓΩ
(1) 0.2mol CxHyΓζ1.2molCO2+1.2molH2OΘ§”…‘≠Ή” ΊΚψΖ÷ΈωΘΜ
(2)A≤ΜΡή ΙδεΥ°Ά …ΪΘ§ΒΪ‘Ύ“ΜΕ®ΧθΦΰœ¬ΡޔꬻΤχΖΔ…ζ»Γ¥ζΖ¥”ΠΘ§Τδ“Μ¬»¥ζΈο÷Μ”–“Μ÷÷Θ§‘ρ÷Μ”–“Μ÷÷HΘ§ΈΣΜΖΦΚΆιΘΜ
(3) ”…Ζ÷Ή”Ήι≥…Ω…÷ΣΘ§…ζ≥…CO2ΚΆH2OΗς3molΘ§ΧΰΈΣ0.75molΘ§Ω…»ΖΕ®ΧΰΒΡ÷ ΝΩΚΆœϊΚΡΒΡ―θΤχΘΜ
(4)»τΧΰAΡή ΙδεΥ°Ά …ΪΘ§‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κH2Φ”≥……ζ≥…Θ§ΤδΦ”≥…≤ζΈοΨ≠≤βΕ®Θ§Ζ÷Ή”÷–Κ§”–4ΗωΦΉΜυΘ§
…ζ≥…ΒΡΆιΧΰΫαΙΙ ΫΈΣ Μρ
Μρ Θ§“‘¥Υ»ΖΕ®AΒΡΫαΙΙΦρ ΫΓΘ
Θ§“‘¥Υ»ΖΕ®AΒΡΫαΙΙΦρ ΫΓΘ
(1) 0.2molΧΰA‘Ύ―θΤχ÷–Άξ»Ϊ»Φ…’ΚσΘ§…ζ≥…CO2ΚΆH2OΗς1.2molΘ§‘ρAΖ÷Ή”÷–Κ§”–CΓΔH‘≠Ή” ΐΖ÷±πΈΣΘΚN(C)=![]() =6Θ§N(H)=
=6Θ§N(H)=![]() =12Θ§AΖ÷Ή” ΫΈΣΘΚC6H12Θ§
=12Θ§AΖ÷Ή” ΫΈΣΘΚC6H12Θ§
“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚC6H12ΘΜ
(2) C6H12÷Μ”–1Ηω≤Μ±ΞΚΆΕ»Θ§»τΧΰA≤ΜΡή ΙδεΥ°Ά …ΪΘ§‘ρΤδΈΣΜΖΆιΧΰΓΘΤδ÷–ΡޔꬻΤχΖΔ…ζ»Γ¥ζΖ¥”ΠΘ§Τδ“Μ¬»¥ζΈο÷Μ”–“Μ÷÷Θ§ΥΒΟςΤδΖ÷Ή”÷–÷Μ”–1÷÷Β»–ßHΘ§Ι ΗΟ”–ΜζΈο «ΜΖΦΚΆιΘ§ΫαΙΙΦρ ΫΈΣΘΚ![]() Θ§
Θ§
“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚ![]() ΘΜ
ΘΜ
(3) »τ»Γ“ΜΕ®ΝΩΒΡΗΟΧΰAΆξ»Ϊ»Φ…’ΚσΘ§…ζ≥…CO2ΚΆH2OΗς3molΘ§”…Ζ÷Ή”Ήι≥…Ω…÷ΣΧΰΈΣ0.75molΘ§÷ ΝΩΈΣ0.75molΓΝ56g/mol=42gΘ§
œϊΚΡ―θΤχΒΡΈο÷ ΒΡΝΩΈΣ0.75molΓΝΘ®4+![]() Θ©=4.5molΘ§
ȩ=4.5molȧ
ΧεΜΐΈΣ4.5molΓΝ22.4L/mol=100.8LΘ§
“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚ42ΘΜ100.8ΘΜ
(4)»τΧΰAΡή ΙδεΥ°Ά …ΪΘ§‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κH2Φ”≥……ζ≥…Θ§ΤδΦ”≥…≤ζΈοΨ≠≤βΕ®Ζ÷Ή”÷–Κ§”–4ΗωΦΉΜυΘ§ΥΒΟςΧΰ÷–Κ§”–C=CΘ§Τδ÷–Κ§”–4ΗωΦΉΜυΒΡ”–3÷÷Θ§ΤδΧΦΦήΫαΙΙΈΣ(ΔΌΔΎΔέ¥ΠΩ…Ζ÷±π≤ΜΆ§ ±Α≤≈≈ΥΪΦϋ)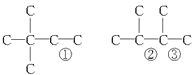 Θ§Ω…Ρή”–ΒΡΫαΙΙΦρ ΫΈΣΘΚ(CH3)3CCH=CH2
Θ§Ω…Ρή”–ΒΡΫαΙΙΦρ ΫΈΣΘΚ(CH3)3CCH=CH2
CH2=C(CH3)CH(CH3)3 (CH3)3C=C(CH3)2 ΘΜ
“ρ¥ΥΘ§±ΨΧβ’ΐ»Ζ¥πΑΗ «ΘΚ(CH3)3CCH=CH2 CH2=C(CH3)CH(CH3)3 (CH3)3C=C(CH3)2ΓΘ


 ΜνΝΠ ‘ΨμœΒΝ–¥πΑΗ
ΜνΝΠ ‘ΨμœΒΝ–¥πΑΗ ΩΈΩΈ”≈ΡήΝΠ≈ύ”≈100Ζ÷œΒΝ–¥πΑΗ
ΩΈΩΈ”≈ΡήΝΠ≈ύ”≈100Ζ÷œΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ0.02molΓΛLΓΣ1ΒΡHCN»ή“Κ”κ0.02molΓΛLΓΣ1ΒΡNaCN»ή“ΚΒ»ΧεΜΐΜλΚœΘ§“―÷ΣΜλΚœ»ή“Κ÷–C(CN-)ΘΦC(NaΘΪ)Θ§‘ρœ¬Ν–ΙΊœΒ÷–Θ§’ΐ»ΖΒΡ «ΘΚ
AΘ°C(NaΘΪ)ΘΨC(CN-)ΘΨC( HΘΪ)ΘΨC(OH-)
BΘ°C(HCN)+C (CN-)=0.04molΓΛL-1
CΘ°C(CN-)ΘΨC(HCN)
DΘ°C(NaΘΪ)+C(HΘΪ)= C(CN-)+C(OH-)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎάφΓΔœψΫΕΒ»Υ°Ιϊ÷–¥φ‘ΎΉ≈““Υα’ΐΕΓθΞΓΘ Β―ι “÷Τ±Η““Υα’ΐΕΓθΞΒΡΖ¥”ΠΓΔΉΑ÷Ο Ψ“βΆΦΚΆ”–ΙΊ ΐΨί»γœ¬ΘΚ
![]()

Υ°÷–»ήΫβ–‘ | ΟήΕ»(gΓΛcm-3) | Ζ–Βψ | œύΕ‘Ζ÷Ή”÷ ΝΩ | |
““Υα | »ή”ΎΥ° | 1.049 2 | 118 | 60 |
’ΐΕΓ¥Φ | ΈΔ»ή”ΎΥ° | 0.809 8 | 117.7 | 74 |
““Υα’ΐΕΓθΞ | ΈΔ»ή”ΎΥ° | 0.882 4 | 126.5 | 116 |
Β―ι≤Ϋ÷η:
Δώ.““Υα’ΐΕΓθΞΒΡ÷Τ±Η
‘ΎA÷–Φ”»κ7.4 g’ΐΕΓ¥ΦΓΔ6.0 g““ΥαΘ§‘ΌΦ”»κ ΐΒΈ≈®ΝρΥαΘ§“Γ‘»Θ§Ζ≈»κ1~2Ω≈Ζ– ·ΓΘΑ¥ΆΦΑ≤ΉΑ¥χΖ÷Υ°ΤςΒΡΜΊΝςΖ¥”ΠΉΑ÷ΟΘ§≤Δ‘ΎΖ÷Υ°Τς÷–‘Λœ»Φ”»κΥ°Θ§ ΙΥ°Οφ¬‘ΒΆ”ΎΖ÷Υ°ΤςΒΡ÷ßΙήΩΎΘ§Ά®»κάδΡΐΥ°Θ§ΜΚ¬ΐΦ”»»AΓΘ‘ΎΖ¥”ΠΙΐ≥Χ÷–Θ§Ά®ΙΐΖ÷Υ°Τςœ¬≤ΩΒΡ–ΐ»ϊΖ÷≥ω…ζ≥…ΒΡΥ°Θ§±Θ≥÷Ζ÷Υ°Τς÷–Υ°≤ψ“ΚΟφΒΡΗΏΕ»≤Μ±δΘ§ Ι”Ά≤ψΨΓΝΩΜΊΒΫ‘≤ΒΉ…’ΤΩ÷–ΓΘΖ¥”Π¥οΒΫ÷’ΒψΚσΘ§ΆΘ÷ΙΦ”»»Θ§Φ«¬ΦΖ÷≥ωΥ°ΒΡΧεΜΐΓΘ
Δρ.≤ζΤΖΒΡΨΪ÷Τ
Α―Ζ÷Υ°Τς÷–ΒΡθΞ≤ψΚΆA÷–Ζ¥”Π“ΚΒΙ»κΖ÷“Κ¬©ΕΖ÷–Θ§Ζ÷±π”Ο…ΌΝΩΥ°ΓΔ±ΞΚΆΧΦΥαΡΤ»ή“ΚΚΆΥ°œ¥Β”Θ§Ζ÷≥ωΒΡ≤ζΈοΦ”»κ…ΌΝΩΈόΥ°ΝρΥαΟΨΙΧΧεΘ§Ψ≤÷ΟΚσΙΐ¬ΥΘ§ΫΪ≤ζΈο≥Θ―Ι’τΝσΘ§ ’Φ·124-126 ΓφΒΡΝσΖ÷Θ§ΒΟΒΫ5.8 g≤ζΤΖΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)άδΥ°”Π¥”άδΡΐΙήΒΡ________(ΧνΓΑaΓ±ΜρΓΑbΓ±)ΩΎΆ®»κΓΘ
(2)≤ζΤΖΒΡΨΪ÷ΤΙΐ≥Χ÷–Θ§ΒΎ“Μ¥ΈΥ°œ¥ΒΡΡΩΒΡ «________________Θ§ΒΎΕΰ¥ΈΥ°œ¥ΒΡΡΩΒΡ «________________Θ§œ¥Β”Άξ≥…ΚσΫΪ”–Μζ≤ψ¥”Ζ÷“Κ¬©ΕΖΒΡ________(ΧνΓΑ…œΩΎΓ±ΜρΓΑœ¬ΩΎΓ±)ΉΣ“ΤΒΫΉΕ–ΈΤΩ÷–ΓΘ
(3)±Ψ Β―ιΧαΗΏ≤ζΤΖ≤ζ¬ ΒΡΖΫΖ® «_________________________________________ΓΘ
(4)≈–ΕœΖ¥”Π÷’ΒψΒΡ“άΨί «_______________________________________________ΓΘ
(5)ΗΟ Β―ιΙΐ≥Χ÷–Θ§…ζ≥…““Υα’ΐΕΓθΞΒΡ≤ζ¬ «_______________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΉΑ÷ΟΦΉΓΔ““ΓΔ±ϊΕΦ «Χζ”κΥ°’τΤχΖ¥”ΠΒΡ Β―ιΉΑ÷ΟΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
ΉΑ÷ΟΦΉ ΉΑ÷Ο““
ΉΑ÷Ο““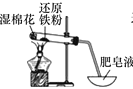 ΉΑ÷Ο±ϊ
ΉΑ÷Ο±ϊ
A.―ÔϱϊΉΑ÷ΟΘ§ Β―ιΫα χ ±œ»“Τ»ΞΨΤΨΪΒΤΘ§‘ΌΫΪΒΦΤχΙήΡΟ≥ωΥ°Οφ
B.ΦΉΉΑ÷Ο÷–¬»Μ·ΗΤΒΡΉς”Ο «≥ΐ»Ξ«βΤχ÷–Μλ”–ΒΡΥ°’τΤχ
C.”Ο““ΉΑ÷Ο Β―ι ±Θ§’τΖΔΟσ÷–≤ζ…ζ¥σΝΩΖ ‘μ≈ίΘ§Βψ»ΦΖ ‘μ≈ίΖΔ≥ω±§Ου…υ
D.»ΐΗωΉΑ÷Οœύ±»ΫœΘ§““ΉΑ÷ΟΦρΒΞΓΔ≤ΌΉςΦρ±ψΓΔΫΎ‘Φ‘≠ΝœΓΔΑ≤»Ϊ–‘ΚΟ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦΘ§ΥΡ÷÷ΉΑ÷Ο÷–Υυ Δ”–ΒΡ»ή“ΚΧεΜΐΨυΈΣ200mlΘ§≈®Ε»ΨυΈΣ0.6mol/LΘ§ΙΛΉς“ΜΕΈ ±ΦδΚσΘ§≤βΒΟΒΦœΏ…œΨυΆ®ΙΐΝΥ0.2molΒγΉ”Θ§¥Υ ±»ή“Κ÷–ΒΡ![]() ”…¥σΒΫ–ΓΒΡΥ≥–ρ «
”…¥σΒΫ–ΓΒΡΥ≥–ρ «
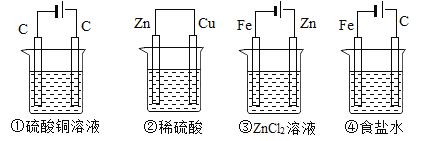
ΔΌΝρΥαΆ≠»ή“Κ ΔΎœΓΝρΥα Δέ¬»Μ·–Ω»ή“Κ Δή ≥―ΈΥ°
A. ΔήΔΎΔΌΔέ B. ΔήΔέΔΌΔΎ C. ΔήΔέΔΎΔΌ D. ΔΌΔέΔΎΔή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “¥”ΚΘ¥χ÷–Χα»ΓΒβΒΡΝς≥Χ»γΆΦΘΚ
![]()
œ¬Ν–≤ΌΉςΉΑ÷Ο≤ΜΖϊΚœ“Σ«σΒΡ «
A.  B.
B. 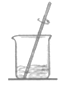 C.
C.  D.
D. 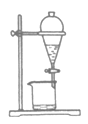
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΒΰΒΣΜ·ΡΤ(NaN3) «“Μ÷÷Έό…ΪΨßΧεΘ§ΙψΖΚ”Ο”ΎΤϊ≥ΒΑ≤»ΪΤχΡ“ΦΑΜ·ΙΛΚœ≥…Β»Θ°≥ΘΦϊΒΡΝΫ÷÷÷Τ±ΗΖΫΖ®ΈΣΘΚ
2NaNH2+N2O®TNaN3+NaOH+NH3Γϋ
3NaNH2+NaNO3®TNaN3+3NaOH+NH3Γϋ
(1)ΔΌΒΣ‘≠Ή”ΒΡL≤ψΒγΉ”≈≈≤ΦΆΦ_____________________ΓΘ
ΔΎΒΣΥυ‘ΎΒΡ÷ήΤΎ÷–Θ§ΒΎ“ΜΒγάκΡήΉν¥σΒΡ‘ΣΥΊΈΣ_____________Θ®Χν‘ΣΥΊΖϊΚ≈Θ©ΓΘ
Δέ”κN3ΜΞΈΣΒ»ΒγΉ”ΧεΒΡΝΘΉ”ΈΣ____________Θ®–¥≥ω“Μ÷÷Θ©ΓΘ
ΔήΑ±ΤχΒΡΒγΉ” Ϋ____________ΓΘ
(2)NH3Ζ–ΒψΘ®©¹33.34ΓφΘ©±»N2OΖ–ΒψΘ®©¹88.49ΓφΘ©ΗΏΘ§Τδ÷ς“Σ‘≠“ρ «____________
(3)“άΨίΦέ≤ψΒγΉ”Ε‘ΜΞ≥βάμ¬έΘ§NO3-ΦδΙΙ–Ά≥ __________–ΈΓΘ
(4)Τϊ≥ΒΑ≤»ΪΤχΡ“ΒΡ…ηΦΤ «Μυ”ΎΖ¥”Π6NaN3+Fe2O3®T3Na2O+2Fe+9N2ΓϋΘ§…ζ≥…Έο÷–ΒΡΧζ «“Μ÷÷≥ΘΦϊΈο÷ Θ§ΕχΧζΒΡΨßΧε”–»ΐ÷÷Ε―ΜΐΖΫ ΫΘ§Τδ÷–ΝΫ÷÷ΒΡΕ―ΜΐΖΫ Ϋ»γΆΦΥυ ΨΘ§œ¬Ν–”–ΙΊΧζΦΑΨßΧεΒΡΥΒΖ®÷–’ΐ»ΖΒΡ «_________ΓΘ
AΘ°Ϋπ τΧζΒΡΒΦΒγ–‘ «”…”ΎΆ®Βγ ±≤ζ…ζΒΡΉ‘”…ΒγΉ”ΉςΕ®œρ“ΤΕ·
BΘ°ΠΝ©¹FeΓΔΠΟ©¹FeΒΡΕ―ΜΐΖΫ ΫΖ÷±π”κΦΊΚΆΆ≠œύΆ§
CΘ°Ω’Φδάϊ”Ο¬ ΠΝ©¹Fe¥σ”ΎΠΟ©¹Fe
DΘ°Ϋπ τΧζΡΎ≤Ω¥φ‘ΎΫπ τΦϋ
(5)ΧζΒΡ…œ ωΝΫ÷÷ΨßΧεΘ®ΠΝ©¹FeΘΚΠΟ©¹FeΘ©ΒΡΟήΕ»±»÷ΒΈΣ___________ΓΘΘ®–¥≥…–Γ ΐΘ§±ΘΝτ2ΈΜ”––ß ΐΉ÷Θ©

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩίμ»χ¬όΕΓ «“Μ÷÷÷ΈΝΤΆγΙΧ–‘ΤΛΖτTœΗΑϊΝήΑΆΝωΒΡ“©ΈοΘ§ΤδΫαΙΙ»γΆΦΥυ ΨΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «

A. Ζ÷Ή”÷–Υυ”–ΧΦ‘≠Ή”‘ΎΆ§“ΜΤΫΟφΡΎ
B. Φ»ΡήΖΔ…ζΦ”≥…Ζ¥”ΠΘ§”÷ΡήΖΔ…ζœϊ»ΞΖ¥”Π
C. Ρή ΙδεΥ°ΓΔΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …ΪΘ§«“‘≠άμœύΆ§
D. 1molίμ»χ¬όΕΓΖ÷±π”κΉψΝΩΒΡNaΓΔ NaHCO3Ζ¥”ΠΘ§≤ζ…ζΤχΧεΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣl©U2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A. ΫΪTiCl4»ή”ΎΥ°ΓΔΦ”»»Θ§ΒΟΒΫ≥ΝΒμTiO2ΓΛxH2OΘ§ΦΧ–χ±Κ…’Ω…ΒΟΒΫTiO2
B. Ω…≤…»ΓΦ”»»’τΖΔΒΡΖΫΖ® ΙFeCl3¥”Υ°»ή“Κ÷–ΫαΨßΈω≥ω
C. ≈δ÷ΤFeCl3»ή“Κ ±Θ§ΈΣΝΥΖά÷Ι»ή“Κ≥ωœ÷ΜκΉ«Θ§Ω…“‘œρ»ή“Κ÷–ΒΈ»κ…ΌΝΩ―ΈΥα
D. ΈΣΝΥ≥ΐ»ΞMgCl2Υα–‘»ή“Κ÷–ΒΡFeCl3Θ§Ω…‘ΎΦ”»»ΫΝΑηΒΡΧθΦΰœ¬Φ”»κMgCO3Θ§Ιΐ¬ΥΚσΘ§‘Όœρ¬Υ“Κ÷–Φ”»κ ΝΩ―ΈΥα
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com