
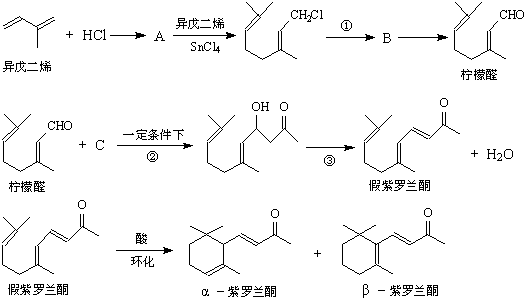
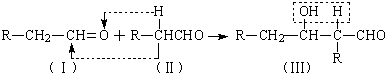
 ,B转化柠檬醛是羟基氧化为醛基;
,B转化柠檬醛是羟基氧化为醛基;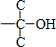 ,核磁共振氢谱显示有5个峰,说明分子中含有5种H原子,
,核磁共振氢谱显示有5个峰,说明分子中含有5种H原子,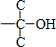 中至少有2种H原子,苯环与剩余的取代基最多含有3种H原子,应为对称结构,另外取代基为(CH3)3C-,且与
中至少有2种H原子,苯环与剩余的取代基最多含有3种H原子,应为对称结构,另外取代基为(CH3)3C-,且与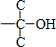 处于对位,或为4个-CH3,
处于对位,或为4个-CH3,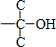 的对位没有甲基.
的对位没有甲基.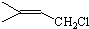 ,由柠檬醛与C的反应产物结构,结合信息②可以确定C的结构简式为:
,由柠檬醛与C的反应产物结构,结合信息②可以确定C的结构简式为: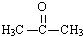 ,故答案为:
,故答案为: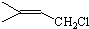 ;
;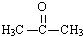 ;
; ,B转化柠檬醛是羟基氧化为醛基,反应方程式为:
,B转化柠檬醛是羟基氧化为醛基,反应方程式为: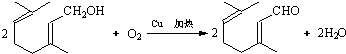 ,
, ;
;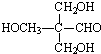 ,故答案为:
,故答案为: ;
;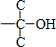 ,核磁共振氢谱显示有5个峰,说明分子中含有5种H原子,
,核磁共振氢谱显示有5个峰,说明分子中含有5种H原子,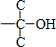 中至少有2种H原子,苯环与剩余的取代基最多含有3种H原子,应为对称结构,另外取代基为(CH3)3C-,且与
中至少有2种H原子,苯环与剩余的取代基最多含有3种H原子,应为对称结构,另外取代基为(CH3)3C-,且与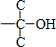 处于对位,或为4个-CH3,且
处于对位,或为4个-CH3,且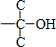 的对位没有甲基,故符合条件的同分异构体共有2种,故答案为:2.
的对位没有甲基,故符合条件的同分异构体共有2种,故答案为:2.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
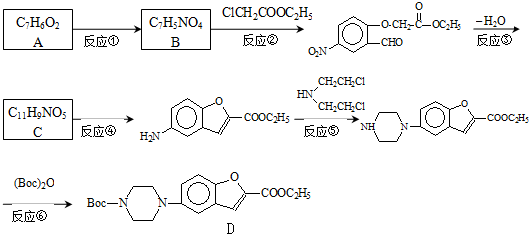
 ;
;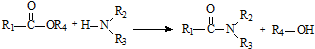 .
. 和
和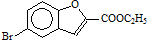 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
 (R,R′为烃基,可以相同,也可以不同)有机物E是重要的有机合成中间体,其合成工艺流程如图:
(R,R′为烃基,可以相同,也可以不同)有机物E是重要的有机合成中间体,其合成工艺流程如图: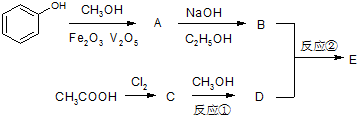
查看答案和解析>>
科目:高中化学 来源: 题型:
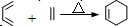
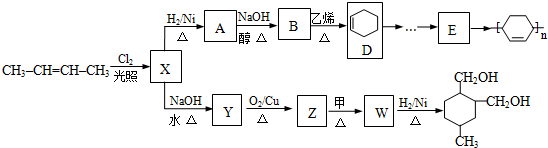
| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作及现象 | 溶液 |
| A | 向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色 | 含有Fe2+溶液 |
| B | 向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 含有CO32-溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | 可能为Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊. | 可能为Ca(OH)2溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 一定条件 |
| [o] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定存在SO32-离子 |
| B、一定存在CO32-离子 |
| C、一定存在Cl-离子 |
| D、可能存在HCO3-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
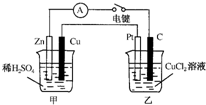 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com