
分析 加入过量盐酸,生成的气体为氢气和二氧化碳,是铝和碳酸镁分别与盐酸反应生成的;加入过量氢氧化钠溶液后生成的沉淀为氢氧化镁,据此可计算出镁元素的物质的量,从而可知碳酸镁、二氧化碳的物质的量,再根据生成气体总体积计算出铝与盐酸反应生成氢气的物质的量,从而可知混合物中铝的物质的量,然后根据m=nM计算出碳酸镁、铝的质量,最后结合混合物总质量计算出氢氧化铝的质量.
解答 解:标准状况下8.96L气体的物质的量为:$\frac{8.96L}{22.4L/mol}$=0.04mol,即铝、碳酸镁与盐酸反应生成氢气和二氧化碳的总物质的量为0.04mol;
再加入过量氢氧化钠溶液后生成的沉淀为氢氧化镁,物质的量为:$\frac{5.8g}{58g/mol}$=0.1mol,
根据质量守恒可知原混合物中含有碳酸镁的物质的量为0.1mol,质量为:84g/mol×0.1mol=8.4g;
0.1mol碳酸镁与过量盐酸反应生成了0.1mol二氧化碳气体,则铝与盐酸反应生成氢气的物质的量为:0.4mol-0.1mol=0.3mol,
根据电子守恒可知原混合物中铝的物质的量为:$\frac{0.3mol×2}{3}$=0.2mol,质量为:27g/mol×0.2mol=5.4g,
原混合物中氢氧化铝的质量为:27.6g-8.4g-5.4g=13.8g,
故答案为:13.8g;8.4g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握质量守恒、电子守恒在化学计算中的应用方法,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:多选题
| A. |  实验室用装置制取氨气 | |
| B. |  装置X若为CCl4,可用于吸收氨气并防止倒吸 | |
| C. |  装置可用于制备氢氧化亚铁并观察其颜色 | |
| D. |  装置是原电池,铁电极为负极,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③④⑤ | C. | ①③⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | NaOH溶液与醋酸溶液反应后所得的pH大于7的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→Cu(OH)2 | B. | CaCl2→CaO | C. | Fe2O3→Fe | D. | Cu(NO3)2→AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2O2中所含阴离子的数目是0.2×6.02×1023 | |
| B. | 标准状况下,2.24L18O2中所含中子的数目是6.02×1023 | |
| C. | 1mol甲烷中含共用电子对的数目是4×6.02×1023 | |
| D. | 电解精炼铜时,当阳极溶解6.4g铜,则转移的电子数为6.02×1022个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中的反应物,不是氧化剂就是还原剂 | |
| B. | 氧化钠是强电解质 | |
| C. | 能导电的物质一定是电解质 | |
| D. | 溶液、胶体这两种分散系的本质区别是否有丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .有机物X的键线式为:
.有机物X的键线式为: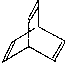


 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com