
【题目】一种第二代抗组胺药物的中间体G的合成路线如下:
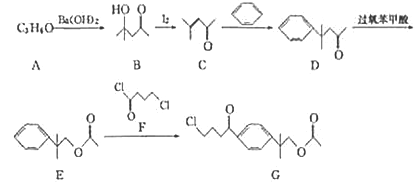
已知:A的分子结构中含有2个甲基。
回答下列问题:
(1)A的名称为__________,由A生成B的反应类型为_______。
(2)G中含氧官能团名称为_______。
(3)F的分子式为_______。
(4)由C生成D的化学方程式为______________。
(5)对二取代芳香化合物W是E的同分异构体,W能发生银镜反应和水解反应,水解产物之一能与FeCl3溶液发生显色反应,则W有________种结构,其中核磁共振氢谱为五组峰,且峰面积之比为1:2 : 2 : 2:9的结构简式为_____________。
(6)参照上述合成路线,以乙醛为原料(无机试剂任选),设计正丁醇的合成路线:_______________________________。
【答案】 丙酮 加成反应 酯基、羰基 C4H6Cl2O  8
8 ![]() CH3CHO
CH3CHO![]()

![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
【解析】(1)根据A的分子式结合A的分子结构中含有2个甲基知A为丙酮(CH3COCH3),A在氢氧化钡存在条件下反应生成B(C6H12O2),为2分子A发生的加成反应,故答案为:丙酮;加成反应;
(2)G( )中的含氧官能团有酯基、羰基,故答案为:酯基、羰基;
)中的含氧官能团有酯基、羰基,故答案为:酯基、羰基;
(3)F(![]() )的分子式为C4H6Cl2O,故答案为:C4H6Cl2O;
)的分子式为C4H6Cl2O,故答案为:C4H6Cl2O;
(4)根据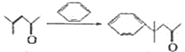 结合CD的分子式可知,C和苯发生加成反应生成D,反应的化学方程式为
结合CD的分子式可知,C和苯发生加成反应生成D,反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(5)对二取代芳香化合物W是E(![]() )的同分异构体,W能发生银镜反应和水解反应,说明W属于甲酸酯,水解产物之一能与FeCl3溶液发生显色反应,说明酯基与苯环连接,则W中含有
)的同分异构体,W能发生银镜反应和水解反应,说明W属于甲酸酯,水解产物之一能与FeCl3溶液发生显色反应,说明酯基与苯环连接,则W中含有![]() 结构,对位基团的化学式为—C5H11,因为有—C5H118种结构,因此W有8种结构,其中核磁共振氢谱为五组峰,且峰面积之比为1:2:2:2:9的结构简式为
结构,对位基团的化学式为—C5H11,因为有—C5H118种结构,因此W有8种结构,其中核磁共振氢谱为五组峰,且峰面积之比为1:2:2:2:9的结构简式为![]() ,故答案为:8;
,故答案为:8;![]() ;
;
(6)以乙醛为原料合成正丁醇,根据A→B→C的反应原理可以使碳链增长,2分子乙醛可以合成出CH3CH=CHCHO,再与氢气加成即可,因此合成路线为CH3CHO![]()

![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH,故答案为:CH3CHO
CH3CH2CH2CH2OH,故答案为:CH3CHO![]()

![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH。
CH3CH2CH2CH2OH。


科目:高中化学 来源: 题型:
【题目】下列有关13C、15N的叙述正确的是( )
A.13C、15N具有相同的中子数B.13C与12C60互为同位素
C.15N的核外电子数与中子数相同D.15N与14N核外电子排布相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曲酸和脱氧曲酸是非常有潜力的食品添加剂具有抗菌抗癌作用,其结构如图所示。下列有关叙述不正确的是

A. 曲酸的分子式为C6H6O4
B. 与脱氧曲酸互为同分异构体的芳香族化合物有4种(不考虑—O—O—键)
C. 曲酸和脱氧曲酸均能使酸性高锰酸钾溶液褪色
D. 脱氧曲酸能发生加成反应和酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 23 g Na与足量H2O反应完全后可生成NA个H2分子(已知:2Na+2H2O===2NaOH+H2↑)
B. 18 g D2O和18 g H2O中含有的质子数均为10NA
C. 标准状况下,22.4 L N2和H2的混合气中含NA个原子
D. 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数小于2NA(已知反应:2NO+O2===2NO2,2NO2![]() N2O4)
N2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用H2还原铁的氧化物并确定其组成的装置如图所示(Zn粒中往往含有硫化物等杂质,焦性没食子酸溶液可吸收少量氧气)。
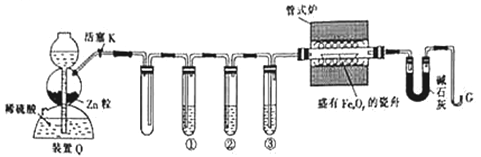
回答下列问题:
(1)装置Q(启普发生器)用于制备H2,还可用于_____(填字母,下同)。
A.生石灰与浓氨水制NH3 B.过氧化钠与水制O2
C.硫化铁固体与稀硝酸制H2S D.大理石与稀盐酸制CO2
(2)①②③中依次盛装的试剂为__________________。
A.KMnO4酸性溶液、浓H2SO4、焦性没食子酸溶液
B.焦性没食子酸溶液、浓H2SO4、KMnO4酸性溶液
C. KMnO4酸性溶液、焦性没食子酸溶液、浓H2SO4
KMnO4酸性溶液中发生反应的离子方程式为_____________。
(3)“加热管式炉”和“打开活塞K”这两步操作应该先进行的是__________,在这两步之间还应进行的操作是_______________。
(4)反应过程中G管逸出的气体是___________,其处理方法是___________。
(5)结束反应时,应该___________,待装置冷却后称量并记录相应数据。
(6)假设反应完全后瓷舟中的固体只有Fe单质,实验中测得了下列数据: ①瓷舟的质量为30.4g;②瓷舟和FexOy的总质量为42.0g;③反应前U形管及内盛物的总质量为98.4g;④反应后U形管及内盛物的总质量为102.0g。由以上数据计算并确定该铁的氧化物的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1 mol Na2CO3·10H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1 mol Na2 CO3(s)溶于水会使溶液温度升高,热效应为△H2;Na2CO3·10H2O受热分解的化学方程式为Na2CO3·10H2O (s) ![]() Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( )
Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( )
A.△H2 <△H3 B.△H1>△H3 C.△Hl+△H3=△H2 D.△H1+△H2>△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯发生的下列反应中,不属于加成反应的是 ( )
A.与氢气反应生成乙烷B.与水反应生成乙醇
C.与溴水反应使之褪色D.与氧气反应生成二氧化碳和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到限度的标志是( )
2AB(g)达到限度的标志是( )
A. 单位时间内生成n mol A2同时生成n mol AB
B. 容器内的总物质的量不随时间变化
C. 单位时间内生成2n mol AB的同时生成n mol B2
D. 单位时间内生成n mol A2的同时生成n mol B2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲知,B点SO2的平衡浓度为0.3mol·L-1
B. 由图甲知,A点对应温度下的平衡常数为80
C. 达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com