
| A. | 18O的原子结构示意图: | B. | 中子数为8的氮原子:${\;}_{8}^{15}$N | ||
| C. | 次氯酸的电子式: | D. | NH4+的结构式: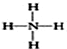 |
分析 A、18O原子的核内有个质子,核外有8个电子;
B、氮原子有7个质子,故中子数为8的氮原子的质量数为7+8=15;
C、HClO中H原子和O原子、O原子和Cl原子间均有一对共用电子对;
D、铵根离子结构中氮原子和氢原子间的配位键是氮原子提供孤对电子,箭头指向氢.
解答 解:A、18O原子的核内有个质子,核外有8个电子,故18O原子结构示意图为 ,故A正确;
,故A正确;
B、氮原子有7个质子,故中子数为8的氮原子的质量数为7+8=15,故氮原子为157N,故B错误;
C、次氯酸为共价化合物,H原子最外层1个电子,Cl原子最外层7个电子,O原子最外层6个电子,则其电子式为: ,故C错误;
,故C错误;
D、NH4+结构中氮原子和氢原子间的配位键是氮原子提供孤对电子,其结构式为: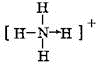 ,故D错误.
,故D错误.
故选A.
点评 本题考查了了电子式、结构式、等化学用语的书写,题目难度中等,注意掌握常见化学用语的概念及书写原则,试题有利于培养学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+3CO=2Fe+3CO2△H=-28.5kJ•mol-1( ) | |
| B. | Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJ | |
| C. | Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=+28.5kJ•mol-1 | |
| D. | Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJ•mol-1. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示
工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:aAm+>bBn+>cCm->dDn- | |
| C. | 离子还原性:aA(n+1)+>bBn+,离子氧化性:cCm->dDn- | |
| D. | 单质还原性:B>A,单质氧化性:D>C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com