
| A. | 对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 | |
| B. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| C. | 升高温度,一般可使活化分子的百分数增大,因而反应速率增大 | |
| D. | 加适宜的催化剂,可使活化分子的百分数大大增加,从而增大反应速率 |
分析 升高温度、加入催化剂,可增大活化分子的百分数,反应速率增大,当活化分子发生碰撞且有生成物生成时,发生化学反应,此时的碰撞为有效碰撞,以此解答.
解答 解:A.对有气体参加的化学反应,增大压强,体系体积减小,则增大气体的浓度,单位体积内活化分子数增加,反应速率增大,故A正确
B.当活化分子发生碰撞且有生成物生成时,发生化学反应,此时的碰撞为有效碰撞,如没有发生化学反应,则不是有效碰撞,故B错误;
C.升高温度,可增大活化分子的百分数,有效碰撞次数增加,反应速率增大,故C正确;
D.加入催化剂,降低反应的活化能,增大活化分子的百分数,有效碰撞次数增加,故D正确.
故选B.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和基本概念的理解和运用的考查,注意外界条件下对化学反应速率的影响,把握有效碰撞的概念,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ;此固体所含化学键类型为离子键、共价键;此固体与AB2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2.
;此固体所含化学键类型为离子键、共价键;此固体与AB2反应的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
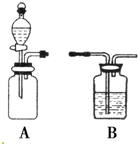 如图是中学化学中常见的实验装置.
如图是中学化学中常见的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制的7个基本物理量之一 | |
| B. | 物质的量可以理解为物质的质量 | |
| C. | 物质的量的单位是“摩尔” | |
| D. | 物质的量是表示物质的数量的单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KMnO4溶液、FeCl3溶液 | B. | 溴水、KMnO4溶液 | ||
| C. | NaOH溶液、FeCl3溶液 | D. | 溴水、Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 析出的氢氧化钠的质量为大于$\frac{40a}{31}$g | |
| B. | 单位体积溶液中OH-个数不变 | |
| C. | 溶液中Na+数目减少 | |
| D. | 氧化钠与水反应生成了碱,所以溶质的质量分数变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
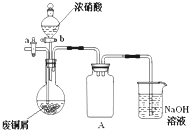 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$ | B. | $\frac{c(N{H}_{4}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | ||
| C. | $\frac{c{H}^{+}}{cO{H}^{-}}$ | D. | c(H+)•c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com