
【题目】某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源B极的名称是________。
(2)如果收集乙装置中两极产生的气体,两极气体的物质的量之比是________。
(3)甲装置中电解反应的总化学方程式:_______________________。
(4)欲用丙装置给铁镀锌,G应该是_______(填“铁”或“锌”),电镀液的主要成分是_______(填化学式)。
(5)装置丁中的现象是___________________
【答案】
(1)负极(2)1∶1;
(3)2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4
2Cu+O2↑+2H2SO4
(4)锌;ZnCl2;
(5)Y极附近红褐色变深
【解析】
试题分析:(1)向乙中滴入酚酞试液,在F极附近显红色,说明该极上氢离子放电,所以该电极是阴极,所以E电极是阳极,D电极是阴极,C电极是阳极,G电极是阳极,H电极是阴极,X电极是阳极,Y是阴极,A是电源的正极,B是原电池的负极;故答案为:负极;
(2)乙池中E为阳极,F为阴极,电解质溶液是氯化钠溶液,电解氯化钠溶液时的阳极氯离子放电生成氯气,阴极是氢离子放电,生成氢气,依据电子守恒可知氯气和氢气的物质的量之比是1:1,故答案为:1:1;
(3)用惰性电极电解硫酸铜溶液时,阳极氢氧根离子放电,阴极是铜离子放电,所以电解反应为:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;故答案为:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4;
2Cu+O2↑+2H2SO4;
(4)用丙装置给铁镀锌,锌作阳极,铁作阴极,ZnCl2作电解质;故答案为:锌;ZnCl2;
(5)根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的粒子会向阴极即Y极移动,所以Y极附近红褐色变深;故答案为:Y极附近红褐色变深。


科目:高中化学 来源: 题型:
【题目】已知在1.01×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.2H2(g)+O2(g)=2H2O(l) ΔH=-484 kJ·mol-1
B.H2O(g)=H2(g)+![]() O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
C.H2(g)+![]() O2(g)=H2O(g) ΔH=-484kJ·mol-1
O2(g)=H2O(g) ΔH=-484kJ·mol-1
D.2H2(g)+O2(g)=2H2O(g) ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国部分城市灰霾天占全年一半,引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3,有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知目前造成我国灰霾天气主要是交通污染。
(1) Zn2+在基态时核外电子排布式为 。
(2) SO42-的空间构型是 (用文字描述)。
(3) PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOX、O3, CH2=CH-CHO, HCOOH, CH3COOONO2(PAN)等二次污染物。
①下列说法正确的是 。
a.N2O结构式可表示为N=N=O
b.O3分子呈直线形
c.CH2=CH-CHO分子中碳原子均采用sp2杂化
d.相同压强下HCOOH沸点比CH3OCH3高,说明前者是极性分子后者是非极性分子
②1mo1PAN中含σ键数目为 。
③NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]S04,该配合物中心离子的配位数为 (填数字).
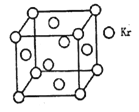
(4)测定大气中PM2.5的浓度方法之一是β一射线吸收法,β一射线放射源可用85Kr,已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则m/n= (填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如右图装置。下列叙述不正确的是( )

A、a和b分别与电源的负极正极相连时,电解氯化钠溶液产生氯气。
B、a和b用导线连接时,碳棒上发生的反应为:O2+2H2O+4e-=4OH-
C、若往溶液中加少许硫酸,无论a和b是否连接,铁片均会溶解,溶液逐渐变成浅绿色
D、若氯化钠溶液改为氯化铵溶液,a和b连接,碳棒上有气泡产生。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是( )
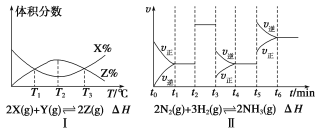

①由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
②由图Ⅱ知,反应在t6时刻,NH3体积分数最大
③由图Ⅱ知,t3时采取减小反应体系压强的措施
④图Ⅲ表示在10 L容器、850 ℃时的反应,由图知,到4 min 时,反应放出51.6 kJ的热量
A.①③ B.②④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸正丁酯是无色透明有愉快果香气味的液体,可由乙酸和正丁醇制备。反应的化学方程式如下:![]()
发生的副反应如下:
有关化合物的物理性质见下表:
化合物 | 密度(g·cm-3) | 水溶性 | 沸点(℃) |
冰乙酸 | 1.05 | 易溶 | 118.1 |
正丁醇 | 0.80 | 微溶 | 117.2 |
正丁醚 | 0.77 | 不溶 | 142.0 |
乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃。
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入11.5mL(0.125mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀。按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸。在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中)。反应基本完成后,停止加热。
方案乙:采用装置乙,加料方式与方案甲相同。加热回流,反应60min后停止加热。

提纯:甲乙两方案均采用蒸馏方法。操作如下:

请回答:
(1)a处水流方向是 (填“进水”或“出水”),仪器b的名称 。
(2)合成步骤中,方案甲监控酯化反应已基本完成的标志是 。
(3)提纯过程中,步骤②是为了除去有机层中残留的酸,检验有机层已呈中性的操作是 ;步骤③的目的是 。
(4)下列有关洗涤过程中分液漏斗的使用正确的是 。
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示
C.放出下层液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中

(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是 ;若按图丁放置温度计,则收集到的产品馏分中还含有 。
(6)实验结果表明方案甲的产率较高,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。
如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-)。

(1)d电极的名称为___________,d电极上的电极反应式为____________________
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1 AgNO3溶液,a电极上的电极反应式为___________,若a电极产生560mL(标准状况)气体,则所得溶液的C(H+)=___________(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入_________(填序号)其物质的量为_______mol
a Ag2O b.AgOH c.AgNO3 d.Ag2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3molP和2.5molQ置于密闭容器中,发生如下反应:3P(g)+Q(g)![]() xM(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(L·min),下列叙述不正确的是
xM(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(L·min),下列叙述不正确的是
A.P的平均反应速率为0.15mol/(L·min)
B.Q的平衡浓度为1mol/L
C.Q的转化率为25%
D.x等于2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】始祖鸟烯形状宛如一只展翅飞翔的鸟,其键线式结构表示如下,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )
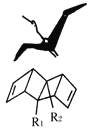
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学式为C12H14
C.若R1=R2=甲基,一定条件下烯烃双键碳原子上的氢也能被取代,则始祖鸟烯的一氯代物有4种
D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则两反应的反应类型是相同的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com