

| ||
| △ |
| ||
| △ |
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象与结论 |
| A | 对某固体进行焰色反应实验 | 火焰呈黄色,说明该物质仅为含钠化合物 |
| B | 向样品溶液中先滴加过量的稀盐酸,再滴加BaCl2溶液 | 先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀,说明样品溶液中一定含有SO42- |
| C | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 | 无砖红色沉淀生成,表明淀粉没有水解生成葡萄糖 |
| D | 向0.1mol?L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热 | 浅红色加深,说明Na2CO3的水解是吸热反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
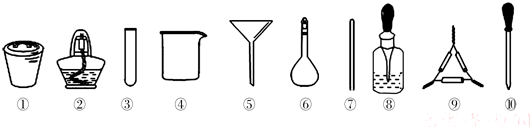
| A、第一步需选用仪器①、②和⑨,①的名称叫钳埚 |
| B、第二步用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦ |
| C、要完成第三步,需选用④、⑤和⑦,除夹持仪器外还缺滤纸 |
| D、第四步,若滤液中含有Fe3+,加入⑧中的溶液后滤液会显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、盛装浓硫酸的仪器的名称为分液漏斗 |
| B、B、D中都可以盛放氢氧化钠溶液,防止污染 |
| C、该装置设计不够严密,可能会出现倒吸 |
| D、析出硫代硫酸钠晶体的方法是蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,它们存在如下转化关系:
由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,它们存在如下转化关系:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在容积为1L的密闭容器中,充入1mol CO2和3mol H2,在温度500℃时发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0.CH3OH的浓度随时间变化如图,下列说法不正确的是( )
在容积为1L的密闭容器中,充入1mol CO2和3mol H2,在温度500℃时发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0.CH3OH的浓度随时间变化如图,下列说法不正确的是( )| A、从反应开始到10分钟时,H2的平均反应速率v(H2)=0.15 mol/(L?min) |
| B、从20分钟到25分钟达到新的平衡,可能是增大压强 |
| C、其它条件不变,将温度升到800℃,再次达平衡时平衡常数减小 |
| D、从开始到25分钟,CO2的转化率是70% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④⑤⑥ | B、①③④⑤ |
| C、①②④⑥ | D、③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X的最高价氧化物对应水化物的酸性比W的弱 |
| B、Y分别与Z、W形成的化合物中化学键类型相同 |
| C、原子半径大小顺序:r(Z)>r(W)>r(X)>r(Y) |
| D、Y的气态简单氢化物的热稳定性比W的弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com