
ij��ѧ��ȤС�������ͼʾʵ��װ�ã�ͼ��ʡ���˼г����������ⶨij��̼�Ͻ�����������������
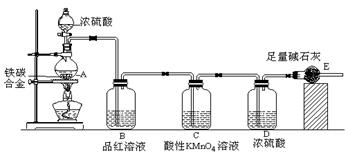
��1��m g��̼�Ͻ��м������Ũ���ᣬδ��ȼ�ƾ���ǰ��A��B��������������ԭ���ǣ�
�ٳ�����̼��Ũ�����Ӧ�� �� ��
��2��д������ʱA��̼��Ũ���ᷢ����Ӧ�Ļ�ѧ����ʽ ��
��3��B�е������ǣ� ��C�������ǣ� ��
��4����A�в����ݳ�����ʱ��ֹͣ���ȣ�����E�����أ�E����b g������̼�Ͻ���������������Ϊ ��д����ʽ����
��5����ͬѧ��Ϊ���ô�װ�ò��������������ƫ������д�����ܵ�ԭ�� ��
��6������װ��������ϴ���ȱ�ݣ����е��²��������������ƫ�͵���
����һ�����ɣ�
 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)____ClO����____Fe(OH)3��____===____Cl����____FeO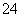 ��____H2O
��____H2O
(2)____MnO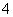 ��____H2O2��____===____Mn2����____O2����____H2O
��____H2O2��____===____Mn2����____O2����____H2O
(3)ij���»�ԭ���Ʊ������մɵ�����(AlN)�ķ�Ӧ��ϵ�е������У�Al2O3��C��N2��AlN��CO��
�뽫AlN֮��ķ�Ӧ����������ֱ��������¿ո��ڣ�����ƽ��
 ��
�� ��
�� �D��
�D��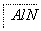 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
21�������ѵ����͡���800�桫1 000��ʱ���TiO2���Ƶ��ѣ�װ������ͼ��ʾ������������ȷ����
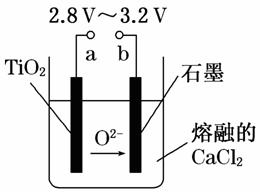
A��aΪ��Դ������
B��ʯī�缫�Ϸ�����ԭ��Ӧ
C�����������ķ�ӦΪ��TiO2��4e��===Ti��2O2��
D��ÿ����0.1 mol�ѣ�ת�Ƶ���0.2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
±�����Ҫ�ɷ���MgCl2�������Fe3+��Fe2+��Mn2+�����ӡ���±��Ϊԭ�Ͽ��Ƶ���������þ��������������ͼ��
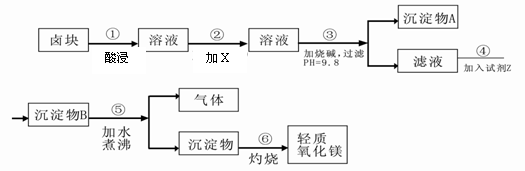
��֪��Fe2+�����������״�����״���Һ�г�ȥ�����Գ���������ΪFe3+������Fe(OH)3������ȥ����Ҫ���Ʒ�����������ʣ�����ݱ�1��2�ṩ�����ϣ���д�հף�
��1 �����������������pH ��2 ��ѧ�Լ��۸��
| �Լ� | �۸�Ԫ/�֣� |
| ƯҺ����NaClO��25.2%�� | 450 |
| ˫��ˮ����H2O2 ,30%�� | 2400 |
| �ռ��98% NaOH�� | 2100 |
| �����99.5% Na2CO3�� | 600 |
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���� �� ��
A����Ԫ����Ҫ�Ե��ʡ�����������ε���ʽ��������Ȼ����
B��þ��������һ���Ŀ���ʴ�ԣ�����Ϊþ�������ױ�����
C��84����Һ����Ҫ�ɷ���NaClO
D��ijЩ����Ԫ�ص���ɫ��Ӧ����ˮ���塢ú��Һ����ʯ�͵��ѻ����ǻ�ѧ�仯�Ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����A�Ƿ����廯���A�����б�������2��ȡ������������֧����A�ĺ˴Ź���������6�����շ壬�������Ϊ1:1:1:1:2:2���ܹ���FeCl3��Һ������ɫ��Ӧ��D�����г���2�����������1����Ԫ�������ǵ�ת����ϵ���£�
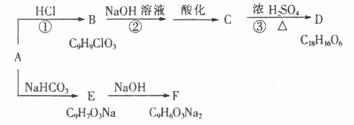
��ش��������⣺
(1)A�����������ŵ�����Ϊ ��
(2)��Ӧ�١������ڼӳɷ�Ӧ���� ������ţ���
(3)B�Ľṹ��ʽ ��D�Ľṹ��ʽ ��
(4)A��E�Ļ�ѧ����ʽΪ ��
(5)��������������A��ͬ���칹���� �֡�
�ٷ����廯��������ϵ�ȡ����������3����
������FeCl3��Һ������ɫ��Ӧ�Ҳ���ˮ�⣻
��lmol�����ʿ���4mol�zAg(NH3)2�{+����������Ӧ��
��lmol�����ʿ���5molH2�ӳɡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͬһ�����ڵ�Ԫ��W��X��Y��Z��ԭ�������������ӡ�����������ȷ����
A�����ʵĻ�ѧ�����ԣ�W��X��Y��Z B��ԭ��������������W��X��Y��Z
C�����ʵ�����������W��X��Y��Z D��Ԫ�ص�����ϼۣ�W��X��Y��Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����л������������ԭ������������ȷ����(����)
A��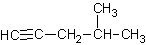 4������1,2����Ȳ
4������1,2����Ȳ
B��CH3 CH (CH3)CH=CHCH3 2������3����ϩ
C��  2, 2, 3��������
2, 2, 3��������
D��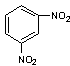 ���������
���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ���ܴ���������� (����)
A����ɫ��Һ�У�ClO����MnO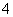 ��Al3����K��
��Al3����K��
B��1.0 mol��L��1��Na[Al(OH)4]��Һ�У�Cl����HCO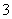 ��K����Ca2��
��K����Ca2��
C����ǿ���Ի����У�[Al(OH)4]����SiO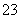 ��Na����K��
��Na����K��
D����ʹ�����Ժ�ɫ����Һ�У�NH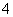 ��[Al(OH)4]����Na��
��[Al(OH)4]����Na��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com