
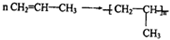
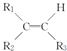
 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$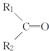 +R3-COOH,
+R3-COOH,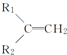 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$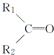 +CO2
+CO2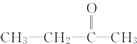 ),则此烯烃的结构简式是CH2=C(CH3)C2H5.
),则此烯烃的结构简式是CH2=C(CH3)C2H5. 分析 (1)丙烯中含有碳碳双键,在一定条件下能发生加聚反应生成聚丙烯;
(2)依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律解答.
解答 解:(1)丙烯中含有碳碳双键,在一定条件下能发生加聚反应生成聚丙烯,反应方程式为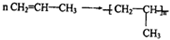 ,该反应为加聚反应,
,该反应为加聚反应,
故答案为: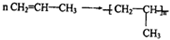 ;
;
(2)乙酸的结构简式为:CH3COOH,丙酸的结构简式为:CH3CH2COOH,依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律可知该烯烃的结构简式为:
CH3-CH=CH-CH2-CH3,
二氧化碳和丁酮(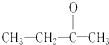 ,依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律可知该烯烃的结构简式为:CH2=C(CH3)C2H5,
,依据烯烃与高锰酸钾酸性溶液反应的氧化产物的规律可知该烯烃的结构简式为:CH2=C(CH3)C2H5,
故答案为:CH3-CH=CH-CH2-CH3;CH2=C(CH3)C2H5.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断及知识迁移能力,明确题给信息断键和成键特点、物质性质是解本题关键,侧重考查烯烃性质,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂又是还原剂 | D. | 既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱和烧碱都属于碱 | |
| B. | 凡是能电离出H+的化合物都叫做酸 | |
| C. | 铝片在空气中能剧烈燃烧并放出大量的热 | |
| D. | NH3的水溶液可以导电,但NH3属于非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的浓度保持恒定 | B. | 混合气体的平均分子量逐渐减少 | ||
| C. | CO和NO的物质的量之比逐渐增大 | D. | v(CO):v(NO):v(N2)=2:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
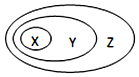 表所列物质或概念间的从属关系符合如图所示关系的是( )
表所列物质或概念间的从属关系符合如图所示关系的是( )| 选项 | X | Y | Z |
| A | 光导纤维 | 酸性氧化物 | 传统无机非金属材料 |
| B | 纯碱 | 碱 | 化合物 |
| C | 电解质 | 化合物 | 纯净物 |
| D | H2SO4 | 含氧酸 | 强酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol H2O的摩尔质量和1mol H2O的摩尔质量 | |
| B. | 200 mL 1 mol•L-1氯化钙溶液中c(Cl-)和100 mL 2 mol•L-1氯化钾溶液中c(Cl-) | |
| C. | 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数 | |
| D. | 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Fe溶于过量稀硝酸,电子转移数为2NA | |
| B. | 标准状况下,2.24L CCl4含有分子的数目为0.1NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 7.8g Na2O2中含有阴离子的数目为0.2NA,与足量水反应时电子转移了0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com